El Síndrome Urémico Hemolítico (SUH) es una entidad clínica definida por la tríada anemia hemolítica no inmune, trombocitopenia e insuficiencia renal aguda, en la que las lesiones subyacentes están mediadas por un proceso de microangiopatía trombótica (MAT) sistémica (1).
La mayoría de los casos de SUH son causados por una infección entérica por Escherichia coli productora de toxina Shiga (STEC) u otros gérmenes productores de verotoxina (VTEC), dando lugar a lo que se conoce como SUH típico o STEC (VTEC)-SUH. Sin embargo, en aproximadamente un 10% de los casos el SUH se produce como consecuencia de una desregulación y/o la activación excesiva de la vía alternativa del sistema del complemento, por causas genéticas o adquiridas (autoanticuerpos), que conduce al desarrollo de daño endotelial y fenómenos de MAT sistémica. Este tipo de SUH relacionado con una desregulación del complemento se denomina SUH atípico (SUHa) (2).
Ante un cuadro clínico sugestivo de MAT, el diagnóstico deberá orientarse hacia SUHa si la prueba de toxina Shiga/STEC es negativa, la actividad plasmática de ADAMTS13 > 5-10% y se descartan formas secundarias de SUH.
Se han descripto mutaciones inactivadoras en genes que codifican reguladores del complemento (factor H, factor I y proteína cofactor de membrana) y mutaciones de ganancia de función en genes que codifican los activadores del complemento (C3 y factor B99) (3). Mutaciones en el gen que codifica la trombomodulina, una glucoproteína unida a la membrana con propiedades anticoagulantes que modulan la activación del complemento en las superficies celulares, también se han descripto en SUHa.
El factor H es una proteína sérica, codificada por el gen CFH (OMIM 134370), que actúa como el principal regulador de la vía alternativa del complemento. Se ha descripto que alrededor del 30% de los pacientes con SUHa presentan mutaciones en el gen CFH, la mayoría corresponde a mutaciones heterocigotas sin sentido que se agrupan en los exones C-terminales, una minoría de las mutaciones en CFH son deleciones o mutaciones sin sentido que resultan en una proteína severamente truncada o una secreción alterada (4).
El gen CFH, se encuentra dentro de un cluster de genes que incluye cinco genes adicionales (CFHR1 a CFHR5) que codifican las proteínas homólogas relacionadas con FH (FHR-1 a FHR-5). El análisis de secuencia de esta región muestra evidencia de varias duplicaciones genómicas grandes, lo que resulta en un alto grado de identidad de secuencia entre CFH y los genes CFHRs haciéndolos susceptibles a generar reordenamientos genómicos mediante recombinación homóloga no alélica. Rearreglos y deleciones en esta región han sido asociados al desarrollo de SUHa (5).
La técnica Gold-standard para la valoración del número de copias es Multiplex ligation-dependent probe amplification (MLPA). En Cibic Laboratorios realizamos el ensayo para la detección de deleciones y/o duplicaciones en los genes CFH, CFHR1, CFHR2 y CFHR3 mediante MLPA.
Prestaciones disponibles en Cibic:
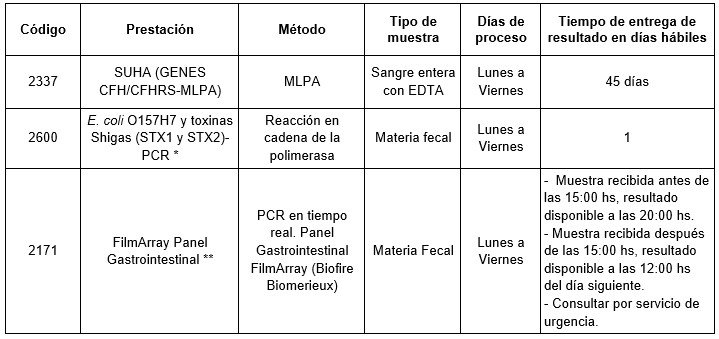
* Detecta por separado la presencia de bacterias E. coli con serotipo O157H7 y las toxinas STX1 y STX2
** Detecta un total de 22 patógenos entre virus, bacterias (entre ellos a E. coli productora de toxinas tipo Shiga STX1/STX2) y parásitos a partir de una única muestra de materia fecal y con un mínimo tiempo de procesamiento
Referencias:
1. Síndrome Urémico Hemolítico. e-NEWS Nro. 480 del 7/8/2019 de Cibic Laboratorios:
2. Josep M. Campistol, et al (2015). Actualización en Síndrome hemolítico urémico atípico: diagnóstico y tratamiento. Documento de consenso. 0211-6995/ 2015. Sociedad Española de Nefrología.
3. Francis N. J. et al (2012). A novel hybrid CFH/CFHR3 gene generated by a microhomology-mediated deletion in familial atypical hemolytic uremic síndrome. BLOOD, 12 JANUARY 2012 VOLUME 119, NUMBER 2.
4. Kavanagh D. et al (2011). Atypical Hemolytic Uremic Syndrome, Genetic Basis, and Clinical Manifestations. Hematology. Am Soc Hematol Educ Program. 2011; 2011:15-20.
5. Zipfel PF, Edey M, Heinen S, et al. Deletion of complement factor H-related genes CFHR1 and CFHR3 is associated with atypical hemolytic uremic syndrome. PLoS Genet. 2007;3(3):e41. doi:10.1371/journal.pgen.0030041.
Para mayor información o consultas:
 Sección: Biología Molecular.
Sección: Biología Molecular.
Lic. Alan Gomez.
Tel 0341-4722424. Interno: 243/225.
 Sección: Biología Molecular.
Sección: Biología Molecular.
Lic. Analía Seravalle.
Tel 0341-4722424. Interno: 242.

