El Herpes Humano tipo 8 (HHV-8), es un virus de ADN, miembro de la familia Herpesviridae, y el único virus humano de la subfamilia Gammaherpesviridae. Está vinculado como agente causal del Sarcoma de Kaposi (SK) y también asociado a la Enfermedad de Castleman multicéntrica (ECM) y al linfoma primario de cavidades o linfoma efusivo primario (LEP).
El HVH8 es capaz de infectar distintos tipos celulares en los que generalmente se encuentra en forma latente como una estructura episómica nuclear. Infecta primariamente las células B, macrófagos, células endoteliales (células ahusadas en las lesiones del SK) y células epiteliales. Luego de la infección aguda puede establecer latencia de por vida.
El HHV-8 adquirió importancia en 1994 en la epidemia de SIDA, cuando fue aislado como agente etiológico del Sarcoma de Kaposi y más tarde como agente causal de Linfoma efusivo primario y algunas formas de Enfermedad de Castleman multicéntrica.
El Sarcoma de Kaposi (SK) es una angiomatosis sistémica de evolución maligna, que se manifiesta primariamente como nódulos vasculares múltiples en la piel y otros órganos. Afecta predominantemente a hombres, es muchísimo más frecuente en personas con sida que en la población general y más del 95% de estos observan en varones homosexuales. El HHV-8 DNA está presente en la mayoría de las células tumorales llamadas células ahusadas en las lesiones.
La Enfermedad de Castleman (ECM) (hiperplasia angiofolicular de los ganglios linfáticos), multicéntrica es un trastorno agresivo y por lo general fatal, con riesgo de complicaciones infecciosas, linfoma maligno y SK. La presencia del HHV8 se asocia con la infección por el VIH, detectándose en el 100% de los casos de MCD en pacientes HIV positivos y cerca del 50% de los casos HIV negativos.
El Linfoma efusivo primario (LEP) es un raro linfoma de células B agresivo que aparece en los pacientes con SIDA principalmente en su cavidad pleural, pericárdica y peritoneal en forma de derrames linfomatosos. Son poco frecuentes. Las células son transformadas completamente por el HHV, observándose episomas en cada célula, lo que ha facilitado el establecimiento de numerosas líneas celulares.
La transmisión del virus ocurre primariamente por saliva pero puede ser transmitida sexualmente por semen y secreciones cervicovaginales, en forma vertical a través de la leche materna o por vía intravenosa por uso de drogas o transfusiones. El HHV8 puede ser transmitido por trasplante de órgano sólido como riñón o corazón o de los hemoderivados administrados.
En las personas trasplantadas, el SK también puede ser el resultado de la reactivación de una infección latente por HHV8 en un receptor previamente seropositivo. La proporción de casos que se adquieren por reactivación o por primoinfección parece relacionada con la prevalencia del HHV8 en la población. Los mecanismos de transmisión dependen de la endemicidad del HHV8 en las distintas regiones.
El HHV8 tiene una distribución mundial pero muestra grandes diferencias entre distintas áreas geográficas. En la mayor parte de África la seroprevalencia supera el 50%. La prevalencia en Asia, Latinoamérica, EEUU y en el norte de Europa es baja, siendo relativamente alta en el sur de Italia.
El diagnóstico debe concentrarse en algunos síndromes o situaciones clínicas en las que caben mayores posibilidades de diagnóstico o anticipación de situaciones clínicas trascendentes para los pacientes. En la actualidad, el mismo puede realizarse mediante la detección del ADN viral por PCR y por métodos serológicos.
Los ensayos serológicos carecen de estandarización y tienen gran variabilidad de la sensibilidad y especificidad, por lo que su utilidad es limitada. Globalmente, el testeo serológico de HHV-8 no se incluye de rutina en el screening pre-trasplante.
La detección directa del ADN viral mediante PCR puede realizarse a partir de las distintas muestras clínicas como saliva o células mononucleares de sangre periférica y semen. Puede realizarse también en material de biopsia de tejido del sitio involucrado como tejido de tumor de SK, nódulo linfoide para ECM o líquido pleural o ascítico en LEP.
La detección de HHV8 mediante PCR debe ser utilizada en conjunto con la presentación clínica patológica para respaldar el diagnóstico y manejo de las enfermedades relacionadas con HHV8.
Prestación disponible en Cibic:
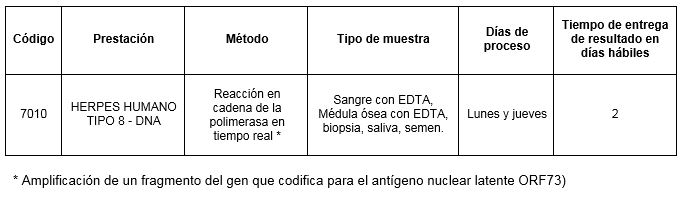
Referencias:
1. De Paoli, P et al. (2004) Herpesvirus 8: an update. Microbes and Infection 6:328-335.
2. Pellett Madan, R., & Hand, J. (2019). Human Herpesvirus 6, 7 and 8 in Solid Organ Transplantation- Guidelines from the American Society of Transplantation Infectious Diseases Community of Practice. Clinical Transplantation, e13518. doi:10.1111/ctr.13518
Para mayor información o consultas:
Dra. Mariela Sciara.
Bioquímica y especialista del área Biología Molecular
Cibic Laboratorios
Teléfono: 0341- 4722424. Interno: 225

