El virus de la Hepatitis B (VHB) es un pequeño virus envuelto con genoma de ADN perteneciente a la familia Hepadnaviridae, principalmente hepatotropo. Su genoma de ADN compacto, parcialmente doble cadena, está organizado en 4 marcos de lecturas que codifican 7 proteínas (estructurales y no estructurales). El análisis de la divergencia de nucleótidos en el genoma viral ha permitido identificar 9 genotipos (A-I) y varios subtipos con diferente distribución geográfica (1).
La probabilidad de que la infección evolucione a la cronicidad depende de la edad a la cual se genere el contacto con el VHB. Así es, como luego de la infección aguda aproximadamente el 5% de los adultos, más del 90% de los neonatos y hasta el 30% de los niños menores de 5 años pueden evolucionar a la cronicidad. Alrededor del 1% de los cuadros sintomáticos agudos pueden desarrollar insuficiencia hepática (2)
Aquellas personas que desarrollan una infección crónica tienen una menor sobrevida que las personas no infectadas debido al desarrollo de complicaciones como cirrosis y hepatocarcinoma (HCC) (3).
A pesar de contar con una vacuna efectiva para prevenir la infección por VHB, la misma continua siendo un serio problema de salud a nivel global. Se estima que alrededor de 257 millones de personas en todo el mundo se encuentran infectadas crónicamente (3). En Argentina y Latinoamérica no hay estadísticas oficiales aunque se estima que en nuestro país la prevalencia podría rondar entre 1 y 2% (4). Se sabe que el genotipo de mayor circulación en nuestro medio es el F, seguido por el A y el D (5).
Como virus no citopático, la inmunopatogenia en la infección por VHB está mediada principalmente por respuestas celulares a proteínas virales expresadas en la superficie del hepatocito, generando la subsecuente lesión hepática. La replicación persistente del VHB puede desencadenar respuestas inmunes fuertes y continuas, provocando daño hepático severo (6). Esto deja a las claras, la necesidad de suprimir la replicación viral en aquellos pacientes con enfermedad hepática avanzada, tal como lo definen las guías Americana, Europea y las publicadas en nuestro medio por el Ministerio de Salud y la Asociación Argentina para el Estudio de las Enfermedades del Hígado (AAEEH) (1), (2), (7), y (8).
Las estrategias de primera línea recomendados por dichas guías, aunque con diferentes matices, son un inmunomodulador como el Interferón pegilado alfa 2a (PEG IFN alfa 2a), o antivirales de acción directa análogos de nucleós(t)idos (NUCs) como Entecavir (ETV) y Tenofovir (TDV) ), dejando relegados a otros NUCs como Lamivudina (LVD), Adefovir-dipivoxil (ADV), Telvibudina (LdT) como opciones ante casos especiales por su baja efectividad y barrera genética en relación a ETV y TDV.
Se encuentra documentada una relación entre el genotipo viral y la respuesta al tratamiento con PEG IFN alfa 2a, así como también entre el genotipo viral y la progresión de la infección, tanto en estadio agudo como crónico. Los pacientes con genotipos A y B tienen una mejor respuesta a la terapia basada en PEG IFN alfa 2a que los pacientes con genotipo C y D (6). Además, en comparación con los genotipos A y B, los pacientes con genotipo C y D tienen un mayor riesgo de desarrollar cirrosis y HCC, lo que conduce a una peor evolución clínica. Mientras que el genotipo F, presente en nuestra población, se asoció con un riesgo mayor de HCC que los genotipos A y D (9).
Debido a la duración prolongada del tratamiento con NUCs y a la alta tasa de error de la polimerasa (RT) viral, es factible la selección de mutaciones de resistencia al tratamiento. Ante un incremento de la carga viral (CV) o a la imposibilidad de lograr CV no detectable, habiendo descartado previamente problemas de adherencia, las guías nacionales e internacionales recomiendan fuertemente realizar el estudio de resistencia para detectar la mutación o mutaciones involucradas en el fallo virológico y así definir el tratamiento más efectivo (1), (7), (8).
En Cibic contamos con un ensayo de PCR seguido de secuenciación directa de un fragmento de 344 aminoácidos de la RT viral. Es una técnica sensible y específica que permite en un mismo estudio definir el genotipo viral, así como la presencia de mutaciones de resistencia a todos los NUCs disponibles en el mercado. Es importante tener en cuenta que para realizar el ensayo es necesario contar con CV mayor a 1000 UI/ml.
Prestación disponible en Cibic:
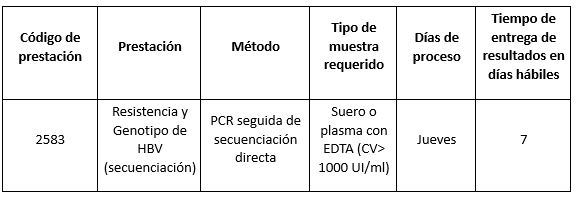
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la extranet.
Referencias:
1. EASL 2017 Clinical practice guidelines: Management of chronic hepatitis B virus infection. J Hepatol. 2017 vol 67: 370–398
2. Recomendaciones para el tratamiento de personas con Hepatitis B Crónica. MINSAL 2013.
3. Ly KN, Xing J, Monina Klevens R et al. The increasing burden of mortality from viral hepatitis in the United States between 1999 and 2007. Ann Intern Med 2012; 156: 271 –278.
4. Global Hepatitis Report 2017. Geneva: World Health Organization; 2017. Licence: CC BY-NC-SA 3.0 IGO.
5. Hepatitis B virus in Buenos Aires, Argentina: Genotypes, virological characteristics and clinical outcomes. Pezzano et al. 2011 Clin Microbiol Infect 17: 223–231.
6. Hepatitis B Virus Genotypes and Variants. Chih-Lin Lin and Jia-Horng Kao. Cold Spring Harb Perspect Med 2015;5:a021436.
7. Consenso Argentino de Hepatitis B 2011. Buenos Aires: AAEEH; 2011.
8. AASLD Guidelines for Treatment of Chronic Hepatitis B. HEPATOLOGY, Vol. 63, No. 1, 2016 TERRAULT ET AL.
9. Livingston SE, Simonetti JP, McMahon BJ, Bulkow LR, Hurlburt KJ, Homan CE, et al. Hepatitis B virus genotypes in Alaska native people with hepatocellular carcinoma: preponderance of genotype F. J Infect Dis. 2007; 195:5–11. [PubMed: 17152003]
Para mayor información o consultas:
Sección: Biología Molecular
 Lic. Javier Alejandro Sfalcin
Lic. Javier Alejandro Sfalcin
Lic.  Alan Gómez
Alan Gómez
Tel: 0341-4499444 Int: 241

