Es factible que, a lo largo de sus vidas, algunas personas desarrollen una patología en la que se requiera el empleo de un tratamiento farmacológico, el cual puede ser, o no, prolongado en el tiempo. Si bien el régimen de dosificación habitual es terapéuticamente efectivo en la mayoría de los pacientes, algunos individuos no experimentan ningún efecto beneficioso e incluso pueden llegar a sufrir toxicidad por el fármaco, lo cual hace que la prescripción eficaz sea un verdadero desafío clínico.
Actualmente se sabe que la efectividad de un agente farmacológico puede estar influenciada por factores endógenos, como la constitución genética de cada individuo, y exógenos como la edad, sexo, talla y dieta. Los factores genéticos se han asociado como la variable más significativa en el metabolismo de ciertos fármacos, explicando entre un 20 y un 95% de la variabilidad fenotípica que puede mostrar un grupo de individuos en respuesta a un determinado tratamiento (1).
Una amplia gama de fármacos clínicamente relevantes, como anticoagulantes orales (warfarina, acenocumarol y fenprocumon), fármacos antidiabéticos (tolbutamida y glipizida), el anticonvulsivo fenitoína, medicamentos antiinflamatorios no esteroideos (diclofenac, ibuprofeno y piroxicam) son metabolizados por la enzima CYP2C9, un miembro de la subfamilia CYP2C del citocromo P450, que es la isoforma más abundante en el hígado (2). Además, CYP2C9 es la encargada de metabolizar una serie de compuestos endógenos, como ácido araquidónico, ácido linoleico y otros xenobióticos no farmacológicos.
El gen, CYP2C9, que codifica la enzima CYP2C9 es altamente polimórfico. Se han descrito muchas variantes, pero las más prevalentes y estudiadas son los polimorfismos CYP2C9*2 y CYP2C9*3.
El alelo CYP2C9*2 es el resultado de una transición C>T en la posición 430 del gen, que conduce a una sustitución Arg por Cys en el residuo 144 de la molécula CYP2C9.
Por otro lado, el alelo CYP2C9*3 es el resultado de una transversión A>T en la posición 1075 del gen, lo que lleva a una sustitución Ile por Leu en el residuo 359 de la molécula CYP2C9.
Ambos alelos conducen a una reducción significativa de la actividad enzimática, por lo que representan la principal causa de disminución de la actividad enzimática de CYP2C9, al menos en poblaciones de origen caucásico (3). Aquellos pacientes con actividad enzimática reducida tienen riesgo de reacciones adversas a fármacos, especialmente para aquellos con una ventana terapéutica estrecha, como warfarina, fenitoína, glipizida y tolbutamida (4).
Determinar el genotipo de CYP2C9 puede resultar en una herramienta útil para el médico tratante, que le ayude en la toma de decisiones terapéuticas guiada en base al genotipo, además de otras variables, y que le permita ajustar la dosis del tratamiento para lograr el efecto deseado, minimizando los efectos secundarios indeseados.
En Cibic Laboratorios contamos con la prestación 2834 – Genotipificación CYP2C9. En el test se usa la secuenciación tipo Sanger y está diseñado para identificar las variantes alélicas CYP2C9*2 y CYP2C9*3.
En el test, la variante alélica CYP2C9*1 (metabolizador normal) se define como ausencia de las variantes alélicas *2 y *3, por lo cual se debe tener en cuenta que, un individuo identificado como portador de una variante alélica *1, podría ser portador de una variante de actividad reducida menos frecuente.
Prestación disponible en Cibic:
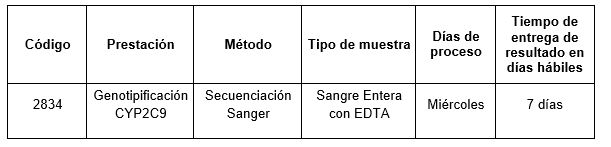
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la extranet.
Referencias
1 – Scott S, Abul-Husn N, Owusu Obeng A, Sanderson S, Gottesman O. Implementation and utilization of genetic testing in personalized medicine. Pharmacogenomics Pers Med. 2014; 7:227-40.
2 – Gardiner SJ, Begg EJ. Pharmacogenetics, drug-metabolizing enzymes, and clinical practice. Pharmacol Rev. 2006; 58: 521–90.
3 – Daly AK, Rettie AE, Fowler DM, Miners JO. Pharmacogenomics of CYP2C9: Functional and Clinical Considerations. J Pers Med. 2017 Dec 28;8(1):1. doi: 10.3390/jpm8010001. PMID: 29283396; PMCID: PMC5872075.
4 – Pirmohamed M, Park BK. Cytochrome P450 enzyme polymorphisms and adverse drug reactions. Toxicology. 2003;192:23–32.
Para mayor información o consultas:
Sección: Biología Molecular
 Lic. Alan Gomez.
Lic. Alan Gomez.
Tel 0341-4861600. Interno: 225
Sección: Biología Molecular
 Lic. Analía Seravalle.
Lic. Analía Seravalle.
Tel 0341-4861600. Interno: 242.

