Las fluoropirimidinas (5-Fluorouracilo [5-FU], capecitabina) se utilizan en el tratamiento de diferentes tipos de tumores sólidos (e.g. cáncer de mama, páncreas, estómago, cáncer colorrectal, esófago, hígado y piel). La enzima dihidropirimidina dehidrogenasa (DPYD, OMIM: 612779) es una enzima crítica en el catabolismo de las bases pirimidínicas uracilo y timina (1).

DPYD cataliza además la detoxificación de agentes quimioterapéuticos basados en compuestos pirimidínicos, drogas de uso frecuente en la terapia de cáncer colorrectal. A nivel hepático, más del 80% del 5-FU se inactiva por acción de DPYD. Una actividad deficiente de la enzima DPYD, dentro del rango terapéutico, se asocia con mielosupresión severa e incluso toxicidad letal, en aquellos pacientes bajo tratamiento con fluoropirimidinas (2, 3).
El gen DPYD se localiza en el brazo corto del cromosma 1 (1p11). La herencia de DPYD es autosómica codominante. Aproximadamente 3% de la población caucásica es heterocigota para una mutación que escinde al exon 14 del gen DPYD, comunmente denominada DPYD-IVS14+1G>A (rs3918290). Esta mutación, origina una molécula de mRNA truncado, con la formación subsecuente de una proteína con actividad enzimática alterada (inactiva). Es importante tener presente que no existe correlación directa entre el genotipo DPYD-IVS14+1G>A y fenotipo (1). Los pacientes heterocigotos para DPYD-IVS14+1G>A, se encuentran en riesgo de desarrollar toxicidad severa al ser tratados con fluoropirimidinas. Aproximadamente un 20% de los pacientes que sufren de toxicidad severa de grado 3 o 4 al tratamiento con 5-FU son heterocigotos para DPYD-IVS14+1G>A (4, 5), siendo esta mutación la más comunmente hallada. La proporción de individuos homocigotos para estas mutaciones es alrededor de 0.1%.
Prestación disponible en Cibic:
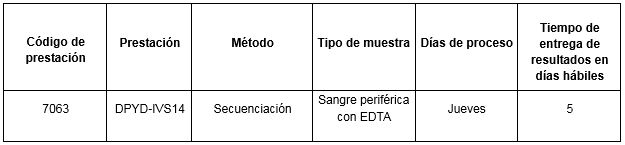
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones.
Bibliografía
1. Van Kuilenburg ABP y cols. Genotype and phenotype in patients with dihydropyrimidine dehydrogenase deficiency. Hum. Genet. 1999; 104:1-9.
2. Meinsma R y cols. Human polymorphism in drug metabolism: mutation in the dihydropyrimidine dehydrogenase gene results in exon skipping and thymine uracilurea. DNA Cell Biol. 1995; 14:1-63
3. Harris BE y cols. Severe 5-fluorouracil toxicity secondary to dihydropyrimidine dehydrogenase deficiency: a potentially more common pharmacogenetic syndrome. Cancer 1991; 68:499-501.
4. Van Kuilenburg AB y cols. High prevalence of the IVS14+1G>A mutation in the dihidropyrimidine dehydrogenase gene of patients with severe 5-fluorouracil-associated toxicity. Pharmacogenetics. 2002; 12:555-8.
5. Raida M y cols. Prevalence of a common point mutation in the dihydropyrimidine dehydrogenase (DPD) gene within the 5′-splice donor site of intron 14 in patients with severe 5-fluorouracil (5-FU)-related toxicity compared with controls. Clin Cancer Res 2001;7:2832–9.
Para mayor información o consultas:
Sección: Biología Molecular
Lic. Analía Seravalle Tel: 0341 4499444 Int: 242
Dra. María Florencia Gosso Tel: 0341 4499444 Int: 258

