La activación de la vía de señalización del receptor del factor de crecimiento epidermal (EGFR) induce procesos involucrados en el desarrollo y progresión tumoral. El EGFR está sobreexpresado en muchos tumores y su expresión esta asociada a la agresividad del tumor, peor pronóstico y resistencia al tratamiento.
En función de esto, el EGFR es uno de los blancos terapéuticos que ha adquirido mayor relevancia en los últimos años. Actualmente están disponibles dos clases de agentes anti-EGFR: i) anticuerpos monoclonales (cetuximab [Erbitux, Merk] y panitumumab [Vectibix, Amgen]) dirigidos contra el dominio extracelular de EGFR, que evitan la fosforilación del receptor y la iniciación de las vías de señalización intracelular RAS/MAPK y (PI3K/Akt), utilizados en el tratamiento de cáncer de colon; e ii) inhibidores de tirosina quinasas (TKIs) (gefinitib [Iressa, Astra Zeneca] y erlotinib [Tarceva, Roche]) los cuales interactúan con el dominio catalítico intracelular del receptor inhibiendo su autofosforilación en la vía de señalización, estos últimos utilizados en el tratamiento de cáncer de pulmón a células no pequeñas (NSCLC) y cáncer de páncreas. La tasa de respuesta con TKIs en pacientes con NSCLC avanzado es del 10 al 20%. A pesar de este bajo %, la evolución clínica en estos pacientes es favorable. Se han identificado mutaciones somáticas activantes específicas dentro del dominio tirosina quinasa de EGFR que se asocian con la respuesta al tratamiento en estos pacientes. Estas mutaciones están principalmente localizadas en los exones 18 (G791A), 19 (deleciones en marco), 20 (pequeñas inserciones o duplicaciones) y 21 (L858R y L861Q). Sin embargo, otra mutación, T790M en el exón 20 se asocia al desarrollo de resistencia. La presencia de mutaciones activantes en estadíos avanzados de NSCLC tratados con TKIs aumenta significativamente la sobrevida libre de progresión y la sobrevida promedio. En ausencia de tales mutaciones activantes, la terapia con TKI no es superior a la terapia convencional. La presencia de la mutación de resistencia T790M al momento de presentación, junto con una mutación activante predice un acortamiento en el tiempo hacia la progresión de la enfermedad. La determinación de mutaciones en los exones 18, 19, 20 y 21 del gen EGFR es útil para predecir la eficacia terapéutica y, por lo tanto, permiten seleccionar aquellos pacientes con cáncer de pulmón que se beneficiarán con estas drogas anti-EGFR.
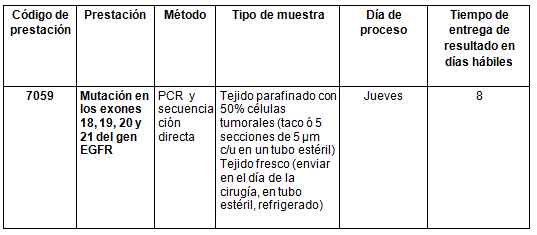
El área de Biología Molecular de CIBIC S.A. continuando con su estrategia de desarrollo científico-tecnológico en materia de diagnóstico médico por laboratorio, incorporó a partir del junio del 2012, la siguiente prestación:
Bibliografía
– Lynch T, Bell DW, Sordella R, Gurubhagavatula S, Okimoto RA, Brannigan BW, Harris PL,Haserlat SM, Supko JG, Haluska FG, Louis DN, Christiani DC, Settleman J, Haber DA. Activating Mutations in the Epidermal Growth Factor Receptor Underlying Responsiveness of Non–Small-Cell Lung Cancer to Gefitinib. N Engl J Med. 350 (21): 2129-2139, 2004.
– Peraldo-Neia C, Migliardi G, Mello-Grand M, Montemurro F, seguir R, Pignochino Y, Cavalloni G, Torchio B, Mosso L, Chiorino G, Aglietta M. Epidermal Growth Factor Receptor (EGFR) mutation analysis, gene expression profiling and EGFR protein expression in primary prostate cancer. BMC Cancer 11:31, 2011.
Para mayor información o consultas:
Dra. María Sonia Baquedano.
Licenciada Analía Seravalle
Tel: 0341 449 9444 interno 242