La presencia de dos grandes barreras inmunológicas debe ser analizada antes de la mayoría de los trasplantes. La primera barrera es la compatibilidad de grupo sanguíneo ABO y la segunda es la presencia de anticuerpos anti HLA preformados en el suero del receptor.
La molécula de HLA tiene más de 300 aminoácidos y puede contener varios epitopes reconocibles por los aloanticuerpos.
Las transfusiones de componentes sanguíneos, trasplantes previos y embarazos conducen a la generación de anticuerpos contra los antígenos HLA, por lo que resulta de vital importancia su estudio previo al trasplante y en el seguimiento post trasplante ya que pueden desencadenar una respuesta de rechazo y pérdida del injerto.
La presencia de anticuerpos anti-HLA preformados en el suero del receptor se puede detectar mediante la técnica de cross match que se basa en el enfrentamiento del suero del receptor del órgano con las células (linfocitos T y B) del donante o con antígenos HLA (purificados o recombinantes) fijados a una fase sólida (ej. mediante la tecnología Luminex).
Esta técnica ha sido una herramienta esencial para facilitar la selección de órganos, de donante y seguimiento post trasplante.
Detección de anticuerpos anti-HLA por Luminex.
Estas técnicas se basan en la búsqueda de anticuerpos preformados fijadores y no fijadores de complemento en el suero del receptor.
El suero del receptor del órgano se enfrenta con antígenos HLA de clase I y II fijados a una fase sólida (suspensión de perlas (beads) de poliestireno con diferente concentración de fluorocromos en su interior). Ante la presencia de anticuerpos anti HLA, estos se unirán a dichas perlas y se pondrán de manifiesto con el agregado de una anti-IgG humana marcada con un fluorocromo (phicoeritrina, PE).
Posteriormente se analiza en un analizador de flujo, Bio-Plex 200® – BIORAD que utiliza tecnología Luminex. Cuando la solución de partículas se adquiere en el Luminex, los haces de láser revelan por una parte el fluorocromo ligado a la anti-IgG y por otra el fluorocromo de la perla al que está asociado. El sistema informático interpreta estas señales, emitiendo un resultado de presencia o ausencia de anticuerpos anti-HLA (Figura 1).
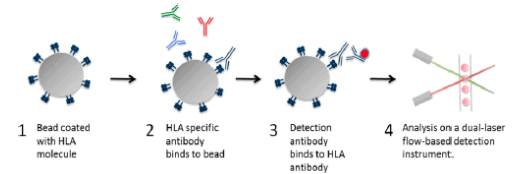
Figura 1. Principio del método de detección de anticuerpos anti HLA por Luminex.
Cibic Laboratorios cuenta con los 3 kits para la detección anticuerpos anti-HLA basados en la técnica Luminex disponibles en el mercado:
1) Screening de anticuerpos
2) Cross match contra panel (PRA ,Panel reactive antibody) y
3) Anticuerpos específicos (DSA, donor-specific antibody).
1) Screening de anticuerpos.
Utiliza para cada perla una mezcla de antígenos HLA de clase I o clase II provenientes de células de varios individuos (Figura 1).

Con este kit se puede determinar la presencia o ausencia de anticuerpos anti HLA clase I y/o II (resultado positivo o negativo).
2) Cross match contra panel (PRA ,Panel reactive antibody).
En este kit los antígenos purificados de un individuo se adhieren a una perla, teniendo así un fenotipo HLA por cada perla (Figura 2).
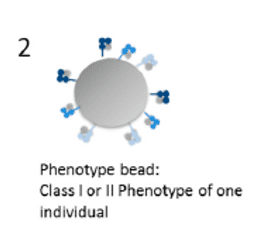 En caso de presencia de anticuerpos arroja un porcentaje de anticuerpos anti clase I y/o II obteniéndose así el valor de PRA (Panel reactive antibody).
En caso de presencia de anticuerpos arroja un porcentaje de anticuerpos anti clase I y/o II obteniéndose así el valor de PRA (Panel reactive antibody).
Ambos kits son utilizados para el ingreso y actualización de pacientes en lista de espera renal, hepatorrenal y renopancreática.
3) Anticuerpos específicos (DSA, donor-specific antibody).
Cada perla contiene múltiples copias de un único antígeno HLA recombinante (SAB, single antigen bead), (Figura 3).
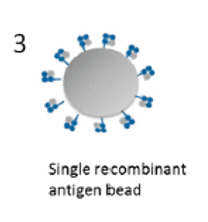
Características de este kit:
– Permite detectar las especificidades individuales HLA.
– Tiene la mayor especificidad y sensibilidad de los 3 kits.
– Es de gran utilidad en estudios pre y post trasplantes de células progenitoras hematopoyéticas y órganos sólidos (renal, hepatorrenal y renopancreático).
Algunas aplicaciones:
– Identificación de mismatches aceptables o no aceptables previos al trasplante (cross match virtual, asignación de antígenos inaceptables en receptores hipersensibilizados en lista de espera para trasplante renal),
– Permite predecir riesgo inmunológico y alternativas de desensibilización, monitoreo inmune post trasplante: permite monitorear la aparición de DSA de novo o incrementos de los DSA pre existentes.
– Permite evaluar la eficacia de los tratamientos del rechazo humoral. Luego del diagnóstico del rechazo humoral la eficacia del tratamiento se sigue evaluando con los métodos de aloanticuerpos.
Prestaciones disponibles en Cibic Laboratorios:
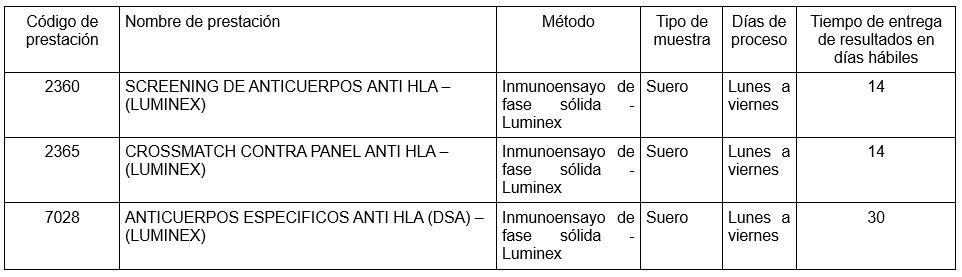
Referencias
1. Enric Carreras ,Carlo Dufour Mohamad Mohty , Nicolaus Kröger, The EBMT Handbook, Hematopoietic Stem Cell Transplantation and Cellular Therapies, Part II Biological Aspects , 9 Histocompatibility, pág 61, 2019.
2. Douglas E. Gladstone and Maria P. Bettinotti, HLA donor-specific antibodies in allogeneic hematopoietic stem cell transplantation: challenges and opportunities, American Society of Hematology, 2017.
3. Delordson Kallon.Histocompatibility & Immunogenetics, A collection of brief revision notes, clinical application, chapter 5 Laboratory techniques, pág 44 – 55, 2011.
4. Delordson Kallon.Histocompatibility & Immunogenetics, A collection of brief revision notes, clinical application, chapter 8 Clinical solid organ transplantation, pág 121 – 155, 2011.
Para mayor información o consultas:
Sección: Biología Molecular
Bioq. Sofía Favot
Tel 0341-486-1600. Interno: 242

