Los Síndromes Mielodisplásicos (SMD) son un grupo de enfermedades clonales de la Stem Cell hematopoyética caracterizada por citopenia, displasia de una o más líneas celulares mieloides, hematopoyesis inefectiva y riesgo aumentado de desarrollar leucemia mieloide aguda. Estas células clonales presentan alteraciones morfológicas, acumulación de anomalías genéticas y diversas alteraciones fenotípicas.
Existen SMD primarios y secundarios según su causa y su incidencia aumentan con la edad, siendo más frecuente entre los 65 y los 70 años
Los criterios mínimos para el diagnóstico de SMD son:
– Prerrequisitos o criterios esenciales: citopenia constante en uno o más de los siguientes linajes: eritroide; neutrófilos; plaquetas. Exclusión de otras causas hematopoyéticas o no hematopoyéticas de desórdenes primarios para citopenias o displasia.
– Criterios decisivos o relacionados: displasia de al menos 10% de todas las células en uno o más linajes en médula osea (MO): mieloide, eritroide, megacariocítico o más de 15% de sideroblastos en anillo. 5-19% de blastos en MO. Anomalías cromosómicas típicas por citogenética convencional o por FISH.
– Co-criterios (para pacientes que cumplen criterios esenciales, pero no criterios decisivos, pero presentan características clínicas típicas de SMD): fenotipo anormal de células (eritroides o mieloides) de MO claramente indicadores de población monoclonal por Citometría de Flujo. Signos moleculares evidentes de población monoclonal. Reducción marcada y persistente de UFC de MO y/o de células progenitoras de SP.
En este tipo de patología, la Citometría de Flujo permite realizar una evaluación cuali-cuantitativa de las diferentes poblaciones celulares de la MO (mieloide, monocítica y eritroide), como así también en los precursores hematopoyéticos CD34+, detectando cambios fenotípicos en los patrones de maduración y diferenciación, pudiendo así definir la existencia de un desorden mieloide clonal.
No existen marcadores ni patrones aberrantes ESPECÍFICOS de SMD
La muestra válida para esta determinación es MO en fresco sin fijador, con anticoagulante EDTA, la cual debe ser remitida al laboratorio antes de las 24 hs de obtención, conservada a temperatura ambiente.
Desde Cibic, a través de la prestación 1524 (Inmunotificación por Citometria de Flujo), disponemos de paneles de anticuerpos monoclonales conjugados con fluorocromos, lo suficientemente amplios para permitir la evaluación de los perfiles fenotípicos de las distintas poblaciones celulares, identificar anomalías fenotípicas y asincronismos madurativos.
Dentro de estos paneles se encuentran antígenos como CD34, CD117, CD13, CD33, HLA-DR que nos permiten evaluar principalmente precursores mieloides.
Además, contamos con otros antígenos tales como: CD71, CD38, CD56, CD2, CD7, CD64, CD14, CD15, CD16, CD11b, CD10, CD20, CD19, CD4; que nos posibilitan caracterizar el resto de los linajes celulares con sus respectivas aberraciones y evaluar la maduración de los mismos.
Junto con los parámetros fluorescentes que nos ayudan en esta identificación, también contamos con otros parámetros: Side Scatter (complejidad celular) y Forward Scatter (tamaño celular), que son fundamentales en la caracterización de los distintos linajes celulares.
En las imágenes debajo, se pueden observar ejemplos de patrones madurativos en médula ósea, normales y patológicos compatibles con SMD, identificados a través de la Citometría de Flujo.
Patrones madurativos normales:
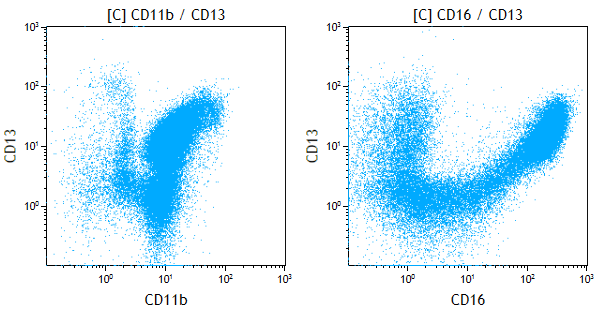
Estos sólo se pueden observar en médula ósea, ya que en sangre periférica solo se encuentran células maduras (no se observan los estadíos previos)
Patrones madurativos alterados
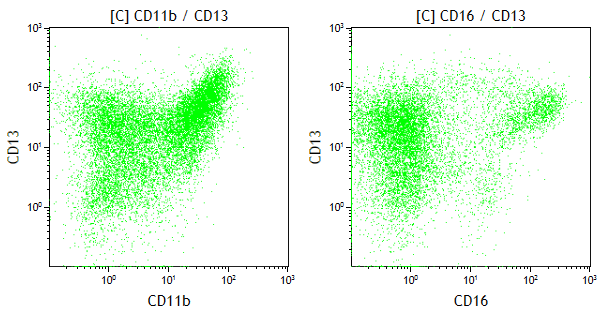
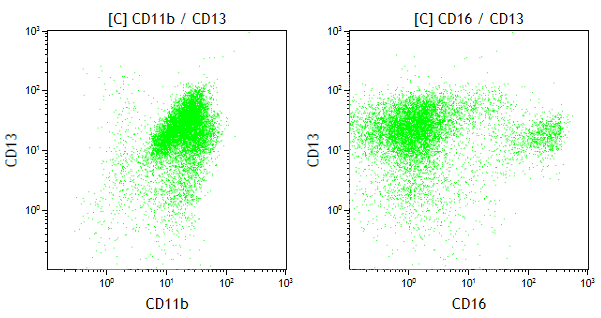
Podemos observar patrones madurativos alterados compatibles con diferentes tipos de SMD, dependiendo del linaje celular afectado.
Prestación disponible en Cibic:
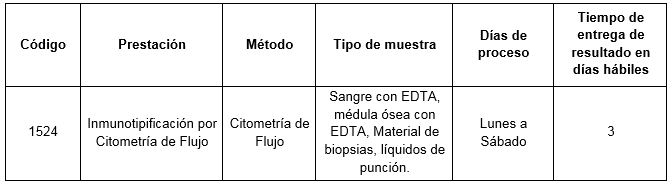
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la extranet.
Referencias:
– Sergio Matarraz, Antonio López. Bone Marrow Cells from Myelodysplastic Syndromes Show Altered Immunophenotypic Profiles That May Contribute to the Diagnosis and Prognostic Stratification of the Disease: a Pilot Study on A Series of 56 Patients. Cytometry Part B (Clinical Cytometry) 78B:154–168 (2010).
-TM Westers, R Ireland. Standardization of flow cytometry in myelodysplastic syndromes: a report from an international consortium and the European LeukemiaNet Working Group. Leucemia 26, 1730 -1741 (2012).
Alex F. Sandes, Daniella M. B. Kerbauy. Combined Flow Cytometric Assessment of CD45, HLA-DR, CD34, and CD117 Expression is a Useful Approach for Reliable Quantification of Blast Cells in Myelodysplastic Syndromes. Cytometry Part B (Clinical Cytometry) 84B:157–166 (2013).
Para mayor información o consultas:
Sector: Citometría de Flujo
Bioq. Mariel Ambrosi
Tel: +54-0341-4722424. int. 259.