El trasplante de células progenitoras hematopoyéticas (CPH) es un procedimiento terapéutico que consiste en tratar de eliminar todas las CPH enfermas de un individuo y reemplazarlas por CPH sanas obtenidas del propio individuo, de donantes familiares/ relacionados o de donantes no relacionados.
Diversas patologías requieren como tratamiento un trasplante de CPH, entre ellas podemos nombrar leucemia linfoblástica aguda (LLA), leucemia mieloblástica aguda (LMA), leucemia mieloide crónica (LMC), síndrome mielodisplásico (SMD), anemia aplásica severa (APS), inmunodeficiencias, linfomas (HODGKIN o NO HODGKIN), anemia de Fanconi, etc.
Las fuentes de CPH pueden ser: médula ósea, sangre periférica o sangre de cordón umbilical y placenta.
La médula ósea ha sido la primera fuente de CPH y la que le dio el nombre al procedimiento. La extracción de estas células requiere de internación del donante, empleo de anestesia general y punción aspirativa reiterada a nivel de ambas crestas ilíacas hasta obtener el número de CPH requerido.
A diferencia de médula ósea, la extracción de sangre periférica no requiere internación. Las células madre no circulan en el torrente sanguíneo y por lo tanto el donante recibe diariamente factores de migración que liberan las CPH de la médula ósea al mismo. La extracción se efectúa al quinto día mediante un procedimiento denominado aféresis en el cual la sangre es procesada en un equipo “programado para retener CPH” que centrifuga, separa elementos y “devuelve” al donante todos los elementos sanguíneos propios no seleccionados.
La sangre que queda en la vena umbilical del cordón y la placenta después de producido el nacimiento es rica en CPH y pueden utilizarse en trasplante. Estas células se recolectan y se criopreservan a la espera de su empleo en un donante compatible. Los trasplantes efectuados con esta fuente han demostrado excelentes resultados, similares a los obtenidos con las fuentes anteriores.
Existen distintos tipos de trasplante de CPH, las dos variantes principales son:
– AUTÓLOGO: cuando las células provienen del mismo individuo.
– ALOGÉNICO: cuando las células provienen de un donante.
Los donantes pueden ser:
1. Donante familiar o relacionado
2. Donante no relacionado
Las moléculas HLA están codificadas por un conjunto de genes, localizados en el brazo corto del cromosoma 6, que se denomina Complejo Mayor de Histocompatibilidad (MHC) y contiene más de 220 genes con funciones diferentes.
Las moléculas HLA de clase I se encuentran codificadas por los genes A, B y C, que darán lugar a la cadena pesada de las moléculas HLA-A, HLA-B y HLA-C, mientras que el gen que codifica la cadena de la β2-microglobulina se encuentra en el cromosoma 15.
Las cadenas alfa y beta de las moléculas HLA de clase II están codificadas por los genes DR, DP y DQ.
Cada nombre de alelo HLA tiene un número único correspondiente a un máximo de cuatro grupos de dígitos separados por dos puntos. Todos los alelos reciben al menos un nombre de cuatro dígitos. En la Figura 1 se representa las recomendaciones actuales de nomenclatura de los alelos HLA.
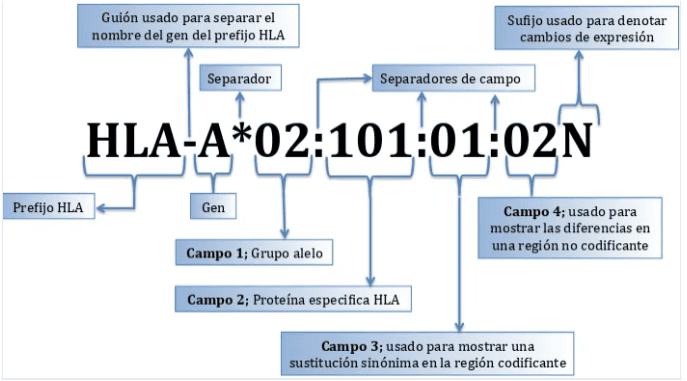
Figura 1. Nomenclatura de los genes del MHC. http://hla.alleles.org/nomenclature/index.html.
Son genes altamente polimórficos y se caracterizan por heredarse de forma codominante de padres a hijos. Su función principal es permitir que el sistema inmune diferencie lo propio de lo extraño y participa también en la comunicación entre células.
El conjunto de genes que se heredan de un progenitor se denomina haplotipo, por lo que cada célula (excepto las células germinales) poseerá un haplotipo paterno y otro materno. Como existen tres genes Clase-I (HLA-A, HLA-B y HLA-C) y cada persona hereda un juego de cada progenitor, cualquier célula de un individuo podrá expresar 6 tipos diferentes de moléculas MHC-I.
En el locus de Clase-II, cada individuo hereda un par de genes HLA-DP (DPA1 y DPA2, que codifican las cadenas α y β), un par de genes HLA-DQ (DQA1 y DQA2, para las cadenas α y β), un gen HLA-DRα (DRA1) y uno o dos genes HLA-DRβ (DRB1 y DRB3, -4 o -5).
Ya que se heredan siguiendo las reglas mendelianas, hay un 25% de probabilidad resultante de que dos hermanos sean genotípicamente idénticos (histoidénticos), es decir, haber heredado el mismo MHC de ambos padres. Los donantes haploidénticos son aquellos que comparten un solo haplotipo y el otro es diferente.
Cuando no es posible obtener células entre hermanos, se recurre a una búsqueda internacional, porque se ha demostrado desde hace varias décadas que compartimos ciertas características inmunológicas con personas con quienes no estamos relacionados familiarmente.
En los últimos años, se han desarrollado nuevos métodos de tipificación de HLA basados en técnicas moleculares, que ofrecen flexibilidad de resolución, reproducibilidad y exactitud superiores al ser comparados con los métodos serológicos tradicionales.
Para los pacientes que requieran un trasplante CPH se solicitará la tipificación en resolución intermedia (PCR SSO) de los locus HLA A, B, C, DR y DQ (grupo alélico y subgrupos posibles englobados en los códigos NMDP) del mismo y de los posibles donantes (hermanos, padres).
El área de Biología Molecular de Cibic Laboratorios ha incorporado un analizador de flujo Bio-Plex 200® – BIORAD que utiliza tecnología Luminex, permitiendo el uso de la metodología PCR-SSO para la genotipificación de los genes HLA.
Es una técnica rápida, que permite analizar 96 muestras en simultáneo y con un nivel de resolución intermedio, permite asignar el grupo alélico y los subtipos posibles están englobados bajo el código NMDP (National Marrow Donor Program).
Esta metodología permite reducir los tiempos de proceso y de análisis, reflejándose en una mejora en los tiempos de entrega de resultados.
Cibic Laboratorios se encuentra habilitado por INCUCAI conforme a la Resolución N°406/15 cumpliendo con los requisitos exigidos por la normativa vigente.
Prestaciones disponibles en Cibic Laboratorios:
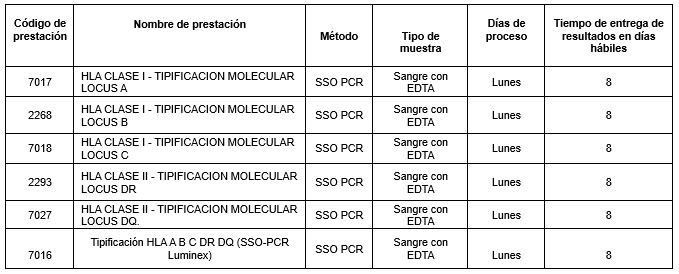
Referencias
1. Enric Carreras ,Carlo Dufour Mohamad Mohty , Nicolaus Kröger, The EBMT Handbook, Hematopoietic Stem Cell Transplantation and Cellular Therapies, Part II Biological Aspects , 9 Histocompatibility, pág 61, 2019.
2. Kathleen Madden & Devon Chabot-Richards.HLA testing in the molecular diagnostic laboratory. Springer-Verlag GmbH Germany, part of Springer Nature 2018.
Para mayor información o consultas:
Sección: Biología Molecular
Bioq. Sofía Favot
Tel 0341-486-1600. Interno: 242