El estudio de cariotipo constitucional es frecuentemente solicitado dentro del testeo preconcepcional de la pareja en tratamiento reproductivo. En conjunto con datos personales, bioquímicos, hormonales y clínicos permiten al profesional médico brindar asesoramiento acerca de opciones de procedimientos, evaluación de riesgos en el embarazo o planeamiento familiar (1-3).
En Cibic Laboratorios estudiamos el cariotipo en linfocitos detenidos en metafase obtenidos a través de cultivo de sangre periférica estimulada con mitógeno. El proceso total que comprende bandeo G, permite visualizar la dotación diploide o conjunto de 46 cromosomas del paciente, donde cada cromosoma presenta un patrón de bandas claras y oscuras que permiten su identificación. Posteriormente son analizados bajo el microscopio de luz trasmitida y con un software especializado para obtener un cariotipo (Figura 1).

Figura 1. Análisis de cariotipo con Microscopio Leica DM 2500 y Software GenASI – Applied Spectral Imagining.
Este cariotipo es un ordenamiento de los 22 pares de autosomas y el par sexual, cuyo estudio permite observar alteraciones numéricas (aneuploidias) y/o estructurales en los cromosomas (Figura 2). La precisión de la técnica de bandeo G está relacionada al nivel de resolución o número de bandas y sub-bandas que es posible distinguir en cada cromosoma. En general, las aberraciones estructurales que pueden ser detectadas corresponden a segmentos mayores a 5 MB. Debe aclararse que no todos los tipos de células están presentes en la muestra que va a ser estudiada, pudiéndose presentar mosaicos a nivel de distintos tejidos somáticos en un mismo paciente (3-5).
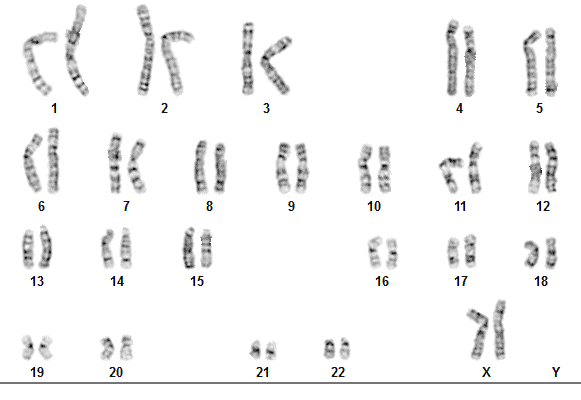
Figura 2. Cariotipo femenino normal 46,XX en sangre periférica.
Las guías internacionales de buenas prácticas en citogenética clínica recomiendan para la técnica de bandeo G alcanzar una resolución mínima de 400 bandas por par haploide para identificación y exclusión de rearreglos estructurales pequeños esperados, pudiéndose alcanzar resoluciones mayores acorde a la calidad de la muestra y capacidad de respuesta del cultivo celular (6-9).
En el enfoque de la pareja subfértil, se suelen realizar hallazgos de cariotipos alterados siendo los más comunes aneuploidias en cromosomas sexuales, traslocaciones balanceadas o deleciones.
En mujeres la anormalidad cromosómica más frecuente son las aneuploidias del cromosoma X (por ejemplo, el Síndrome de Turner 45,X o variantes en mosaico). Así mismo, pueden hallarse alteraciones estructurales del cromosoma X y presencia del cromosoma Y.
En hombres que presentan azoospermia u oligospermia se han identificado cariotipos con desbalance de cromosomas sexuales (por ejemplo, el Síndrome de Klinefelter 47,XXY y mosaicos 47,XXY/46,XY en distintas proporciones). También en menor cantidad rearreglos del cromosoma Y (3,6).
Así mismo, es recomendable realizar cariotipo constitucional en pacientes con amenorrea primaria o secundaria o menopausia prematura, anormalidades espermáticas o enfermedades recesivas ligadas al cromosoma X.
En el caso de pérdidas gestacionales recurrentes o antecedentes de hijos con diagnóstico de enfermedades cromosómicas se aconseja realizar estudio del cariotipo parental (6-9).
El análisis de FISH (del inglés, Hibridación In Situ Fluorescente) es una técnica de mayor sensibilidad con respecto al cariotipo convencional que posibilita identificar regiones específicas de ADN de hasta 150 KB aproximadamente, gracias a la hibridación de sondas de ADN marcadas con fluoróforos que luego son analizadas bajo el microscopio de epifluorescencia. Este proceso puede realizarse tanto en cromosomas en interfase como en metafase de linfocitos de sangre periférica (Figura 3).
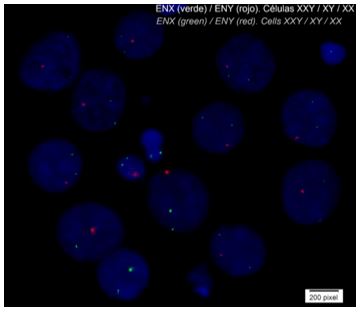
Figura 3. FISH en células en interfase mostrando 3 líneas celulares 47,XXY/46,XY/46,XX. Sondas de región pericentromérica de cromosomas X e Y – LiVeLexel.
El uso de FISH es sugerido para identificar microarreglos no detectables por análisis de bandeo de rutina, para determinar genes involucrados en los puntos de corte tanto en traslocaciones, como microdeleciones y microduplicaciones; también para confirmar posibles mosaicos bajos previamente diagnosticados por citogenética convencional (3, 7-9).
Prestaciones disponibles en Cibic:
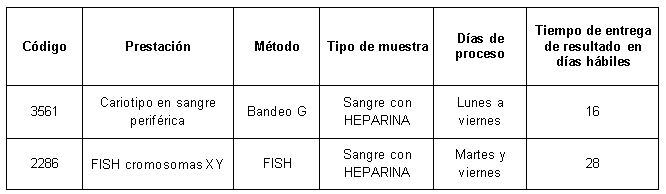
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la extranet.
Referencias
(1) Dra. Susana Kopelman, y cols. Enfoque Inicial de la pareja Infértil. Grupo de Trabajo para Normatizaciones SAMeR, Sociedad Argentina de Medicina Reproductiva. http://www.samer.org.ar/otras_publicaciones.asp
(2) Beth A. y cols. Preconception and prenatal testing of biologic fathers for carrier status. ACMG American College of Medical Genetics Practice Guideline. February 2006 _ Vol. 8 _ No. 2
(3) McKinlay Gardner R. J. y cols. Chromosome Abnormalities and Genetic Counceling 4th Edition. Oxford University Press USA-2011.
(4) Arsham MS. y cols. The AGT Cytogenetics Laboratory Manual 4th Edition. (2017) Wiley-Blackwell.
(5) Software GenASI- Applied Spectral Imagining. Capture and Analysis V.7.2.
(6) Dra. Susana Kopelman y cols. Aborto recurrente (o pérdida recurrente del embarazo). Grupo de Trabajo para Normatizaciones SAMeR. Sociedad Argentina de Medicina Reproductiva. http://www.samer.org.ar/otras_publicaciones.asp
(7) General Genetic Laboratory Reporting Recommendations. Recommendations updated by the Association for Clinical Genomic Science (ratified by ACGS Quality Subcommittee on 24/02/20). Version 1.1.
(8) Ros Hastings y cols. E.C.A General Guidelines and Quality Assurance Cytogenetics. – European Cytogeneticists Association. Newsletter No. 29 January 2012.
(9) Ros Hastings y cols. Specific Constitutional Cytogenetics Guidelines. E.C.A. – European Cytogeneticists Association Newsletter, No. 30, July 2012.
Para mayor información o consultas:
Sección: Citogenética
Dr. Mariano M. Gonzalez. Tel: 0341-4722424. Int: 227
Lic. Ma. Luján Ortiz. Tel: 0341-4722424. Int: 283
Tec. Victorina Carbone.Tel: 0341-4722424. Int: 261

