La histamina (2-[4-imidazol]-etilamina) es una amina biógenica que se forma a partir de la L-histidina en casi todos los órganos y tejidos utilizando la enzima L-histidina descarboxilasa. Aproximadamente el 5% de la cantidad total de histamina ingresa al cuerpo a través de la ingesta de alimentos, mediada por microorganismos intestinales (la llamada histamina exógena). Este metabolito desempeña múltiples efectos en órganos y sistemas del cuerpo humano, ya que actúa favoreciendo funciones fisiológicas a nivel gastrointestinal, genitourinario, respiratorio, cardiovascular, cutáneo, sistema nervioso central e inmunohematológico (1).
En el cuerpo humano, existen dos vías principales para la degradación de la histamina, que involucran la enzima diamino-oxidasa (DAO, sinónimo de histaminasa) o la histamina-N-metiltransferasa. La DAO se sintetiza principalmente en la mucosa del colon pequeño y ascendente, la placenta y los riñones, se acumula en vesículas intracelulares y luego ingresa al espacio extracelular, donde degrada la histamina. Allí, la DAO realiza una “función de barrera”, al limitar el paso de la histamina desde los intestinos a la sangre (2). Por otro lado, la histamina-N-metiltransferasa regula el contenido de histamina dentro de las células, mediante metilación, y está presente en la mayoría de los tejidos (2).
Numerosos estudios informan que una deficiencia de DAO (ya sea de origen genético, patológico o farmacológico) para catabolizar la histamina produce intolerancia a la histamina (IH) lo cual se ha asociado a una amplia gama de trastornos neurológicos, gastrointestinales o epidérmicos (3).
La enzima DAO es codificada por el gen AOC1, para el cual se han descrito variantes de variantes polimórficas de nucleótido único (mayormente conocidas como SNPs), algunas de ellas asociadas a niveles reducidos de actividad DAO.
Específicamente, los SNPs más relevantes que afectan la funcionalidad de la enzima DAO en individuos caucásicos son c.47C>T (p.T16M, rs10156191), c.995C>T (p.S332F, rs1049742) y especialmente c.1990C>G (p.H664D, rs1049793). En la mayoría de los casos, el efecto de estas variaciones genéticas en la funcionalidad de la DAO es a través de cambios en la cinética enzimática, provocando una reducción en la tasa de degradación de la histamina. Por otro lado, también se ha identificado un SNP en la región promotora del gen que provoca una menor actividad transcripcional c.-691G>T (rs2052129) (3).
La existencia de este componente genético relacionado al déficit de DAO, sumado a una serie de estudios que demuestran una asociación entre estos polimorfismos en AOC1 con patologías como migraña o fibromialgia (4, 5 y 6) es que se propone a la determinación de los mismos como una de las estrategias para caracterizar a la población como genéticamente susceptible a la histamina, lo cual puede mejorar la calidad de vida y el tratamiento de los síntomas en pacientes con estas patologías.
En Cibic Laboratorios, desarrollamos la prestación Deficit de DAO (Gen AOC1 – Polimorfismos) en la cual mediante secuenciación Sanger evaluamos los polimorfismos más frecuentes en población caucásica asociados a deficiencia en el catabolismo de la histamina por parte de la enzima DAO.
Estos son:
• c.47C>T (p.T16M, rs10156191)
• c.995C>T (p.S332F, rs1049742)
• c.1990C>G (p.H664D, rs1049793) y
• c.-691G>T (rs2052129)
Prestación disponible en Cibic Laboratorios:
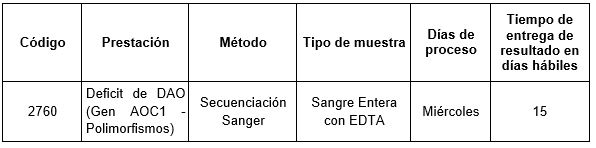
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la extranet.
Referencias
1 – Patel RH, Mohiuddin SS. Biochemistry, Histamine. [Updated 2023 May 1]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK557790/.
2 – Shulpekova YO, y cols. Food Intolerance: The Role of Histamine. Nutrients. 2021 Sep 15;13(9):3207. doi: 10.3390/nu13093207. PMID: 34579083; PMCID: PMC8469513.
3 – Comas-Basté O. y cols. Histamine Intolerance: The Current State of the Art. Biomolecules. 2020;10:1181. doi: 10.3390/biom10081181.
4 – Sukhvinder Kaur y cols. Association of Diamine oxidase (DAO) variants with the risk for migraine from North Indian population, Meta Gene, Volume 24, 2020, 100619, ISSN 2214-5400, https://doi.org/10.1016/j.mgene.2019.100619.
5 – Okutan G y cols. Prevalence of Genetic Diamine Oxidase (DAO) Deficiency in Female Patients with Fibromyalgia in Spain. Biomedicines. 2023 Feb 22;11(3):660. doi: 10.3390/biomedicines11030660. PMID: 36979637; PMCID: PMC10044988.
6 – Okutan G. y cols. Cumulative effect of AOC1 gene variants on symptoms and pathological conditions in adult women with fibromyalgia: a pilot study. Front Genet. 2023 Jun 9;14:1180777. doi: 10.3389/fgene.2023.1180777. PMID: 37359379; PMCID: PMC10288193.
Para mayor información o consultas:
Sección: Biología Molecular
Lic. Alan Gomez.
Tel +54 (341) 4861600 (Int. 225)
Lic. Analía Seravalle.
Tel +54 (341) 4861600 (Int 242)

