El virus de Epstein-Barr (VEB), también denominado virus del herpes humano tipo 4 (HVH-4), es uno de los virus humanos más comunes. El VEB es un virus de doble cadena de ADN lineal encerrado por una cápside proteica, linfotrópico. Pertenece a la familia Herpesviridae, subfamilia gamma de los herpesvirus. La seroprevalencia en adultos mayores de 25 años es > 95% (1). El virus se transmite principalmente por la saliva, aunque también se ha observado transmisión por vía sexual, trasplante o productos sanguíneos que contenían linfocitos (2) (3). El VEB es el agente causante de la Mononucleosis Infecciosa (MI) y también se asocia con el Linfoma de Burkitt y el carcinoma nasofaríngeo.
Durante el ciclo lítico (infección productiva), el virus se replica en los linfocitos B y en células epiteliales de las glándulas salivales y de la mucosa bucal, y se secreta en la saliva. Después de la infección primaria, el VEB permanece en los linfocitos B en estadio de infección latente (sin producción de viriones). Las reactivaciones son frecuentes durante la vida, aunque no constituyen datos clínicos relevantes en huéspedes inmunocompetentes. Después de la infección primaria, el virus se secreta durante toda la vida en la saliva, de manera intermitente. Las infecciones por VEB en niños son a menudo asintomáticas, mientras que del 35% al 50% se convierten en MI en adolescentes. El periodo de incubación es de 4 a 6 semanas.
El diagnóstico de MI puede establecerse en presencia de la tríada: fiebre, faringitis y linfadenopatía, junto con los resultados hematológicos. Los análisis serológicos se utilizan para la estadificación de la infección, para diferenciar la infección por el VEB de otras infecciones con síntomas clínicos similares, por ejemplo infecciones por Citomegalovirus, Toxoplasma Gondii, virus de la hepatitis A, HIV, etc. (4) y para determinar el estado inmunológico en donantes y receptores de trasplantes.
Para determinar el estadio de la infección, se utilizan habitualmente análisis para la detección de anticuerpos IgM e IgG frente al antígeno de la cápside (VCA, viral capsid antigen) del VEB, y los anticuerpos IgG frente al antígeno nuclear 1 del virus Epstein-Barr (EBNA-1) (5). En pacientes con infecciones primarias agudas, generalmente se encuentran anticuerpos IgG e IgM anti-VCA y ausencia de anticuerpos IgG anti-EBNA-1. Los anticuerpos anti-antígenos tempranos anti- EA IgG (EA, early antigen) también son detectables en un 70 – 85% de pacientes con MI en fase aguda aunque son más tardíos que los anti- VCA IgM; alcanzan el máximo entre la tercera y cuarta semana de evolución de la enfermedad y persisten de 3 a 6 meses. Por el contrario, las infecciones pasadas se caracterizan por la presencia de anticuerpos IgG anti-VCA e IgG anti-EBNA 1, y la ausencia de anticuerpos IgM anti-VCA. En algunos casos, los anticuerpos IgM anti-VCA permanecen más tiempo, hasta que ya se han producido los anticuerpos IgG anti-EBNA 1. La serología puede complicarse porque algunos individuos no producen anticuerpos IgM anti-VCA durante la infección primaria, y porque algunos carecen de anticuerpos IgG anti-EBNA 1 (ya sea porque no responden al EBNA-1 o porque han perdido los anticuerpos IgG anti-EBNA 1 por razones como la inmunosupresión) algunas veces años después de la infección primaria o incluso sólo meses después de ella (6). En estos casos es necesario el uso de otros métodos diagnósticos.
Para la determinación fiable del estadio de la infección los ensayos EBV VCA IgM, EBV VCA IgG y EBNA-1 IgG se deben evaluar en paralelo, como se muestra en la tabla a continuación.
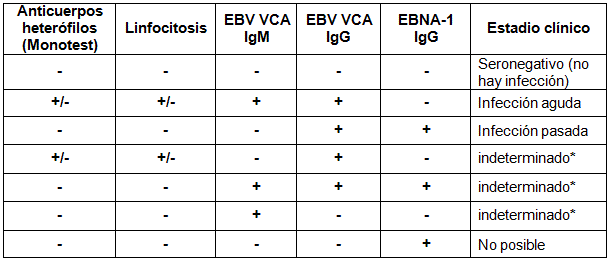
*en estos casos es necesario el uso de otros métodos diagnósticos como es la reacción en cadena de la polimerasa (PCR)
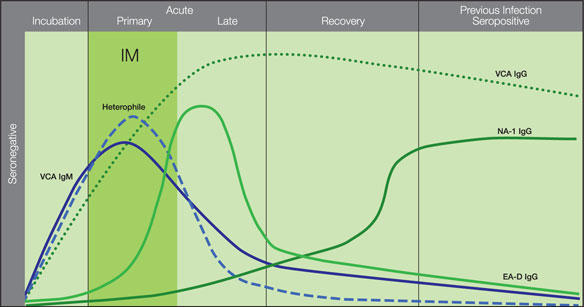
Cinética de los anticuerpos anti-EBV durante y luego de la infección por el virus Epstein-Barr.
Prestaciones disponibles en Cibic:
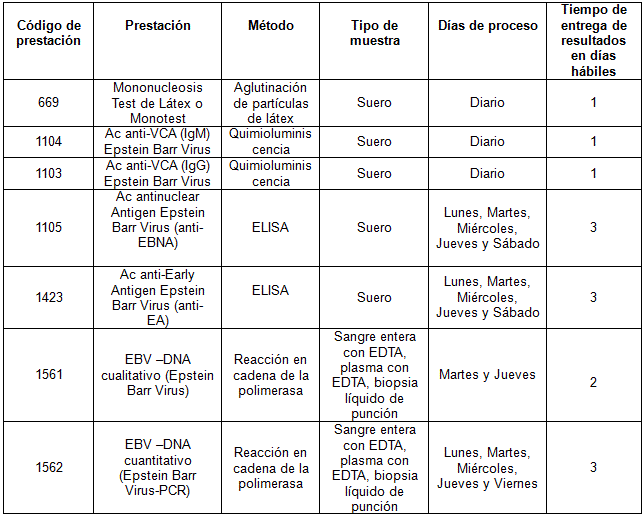
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones.
Bibliografía
1. Rickinson AB, Kieff E. Epstein-Barr virus. In: Knipe PM, Howley DE, Griffin MA, et al., eds. Fields virology, 4th ed. Philadelphia, PA 2001; 2575-2627.
2. Crawford DH, Swerdlow AJ, Higgins C, McAulay K, Harrison N, Williams H, Britton K, Macsween KF. Sexual history and Epstein-Barr virus infection. J. Infect. Dis 2002; 186:731-736.
3. Schooley RT. Epstein-Barr virus (infectious mononucleosis). In: Mandell GL, Bennett JE, and Dolin R, eds. Mandell, Douglas, and Benett’s principles and practice of infectious diseases, vol. 2, 4th ed. Churchill Livingstone, New York, NY 1995; 364-1377.
4. Berth M, Bosmans E. Comparison of three automated immunoassay methods for the measurement of Epstein-Barr virus-specific immunoglobulin M. Clin Vaccine Immunol 2010; 17:559-563.
5. De Ory F, Guisasola ME, Sanz JC, García-Bermejo I. Evaluation of Four Commercial Systems for the Diagnosis of Epstein-Barr Virus Primary Infections. Clin Vaccine Immunol 2011; 18:444-448.
6. Hess RD. Routine Epstein-BarrVirus Diagnostics from the Laboratory Perspective: Still Challenging after 35 Years. J Clin Microbiol 2004; 42(8): 3381-3387.
Para mayor información o consultas:
Bioq. Franco Delleppiagge
Sección: Producción Analítica No Automatizada
Teléfono: 0341 – 4499444. Interno: 220
