La leucemia mieloide aguda (LMA) es una neoplasia maligna con marcada diversidad y heterogeneidad genética, evolución clínica y pronóstico. Resulta de la proliferación clonal de células precursoras hematopoyéticas anormales con diferentes grados de diferenciación, que infiltran la médula ósea y en ocasiones, otros órganos o sistemas (1).
En las últimas décadas, se han identificado anomalías cromosómicas recurrentes y variantes genéticas que constituyen la base para la clasificación y estratificación de riesgo de estas patologías. Esto ha permitido que el tratamiento de los pacientes se realice adaptado al riesgo, guiado por el perfil citogenético y molecular de los clones leucémicos (2).
En el desarrollo hematopoyético normal las células utilizan un complejo sistema de control de la proliferación, diferenciación y muerte celular. El control de la proliferación, en parte, depende de la estimulación de receptores tirosina kinasa inducida por sus ligandos, generándose la activación de una cascada de proteínas quinasas con la consiguiente transmisión de señales desde el medio externo al núcleo de la célula. Diversos estudios han demostrado que el gen FLT3 (FMS-like tyrosine kinase 3) está implicado de forma importante en el control de la hematopoyesis normal (3).
En la actualidad se han descrito mutaciones en el gen FLT3 que originan la auto activación del receptor, pudiendo estas mutaciones contribuir a la progresión leucémica. Estas mutaciones, son las alteraciones genéticas más frecuentes en LMA. Incluyen las duplicaciones internas en tándem (FLT3-ITD) y las mutaciones en el dominio quinasa D835 o I836 (FLT3-TKD) cuyas frecuencias son 30 y 10% respectivamente. Las duplicaciones internas en tándem son las de mayor importancia pronóstica (4).
A pesar del desarrollo creciente de fármacos dirigidos a blancos moleculares específicos, la LMA sigue teniendo alta tasa de morbilidad y mortalidad relacionada a la toxicidad farmacológica y a las recaídas tempranas.
Los diferentes índices pronósticos ayudan a identificar pacientes con alto riesgo de recaída y enfermedad resistente.
Las mutaciones de tipo ITD en el gen FLT3 han sido asociadas con mal pronóstico y han adquirido un rol importante en la toma de decisiones sobre tratamiento. Es por ello la importancia de su detección temprana, así como su correcta determinación por una técnica adecuada que permita evaluar el ratio entre el alelo ITD mutado y el no mutado ya que los pacientes con un ratio <0.5 (bajo) tienen un riesgo comparable a FLT3 no mutado (5).
Prestación disponible en Cibic Laboratorios:
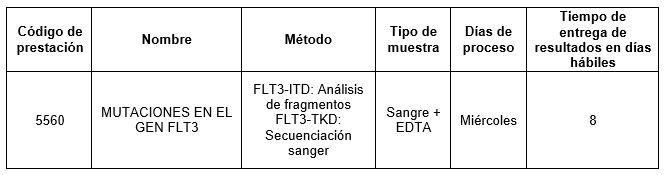
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la extranet.
Referencias
1- Dohner H, Weisdorf DJ, Bloomfield CD. Acute myeloid leukemia. N Engl J Med. 2015;373:1136-52.
2- Grmwade D, Mrozek K. Diagnostic and prognostic value of cytogenetics in acute myeloid leukemia. Hematol Oncol Clin North Am. 2011;25:61.
3- * 136351 fms-related tyrosine kinase 3; FLT3. OMIM web 1, 1–7 (2018).
4- Stirewalt DL, Radich JP. The role of FLT3 in haematopoietic malignancies. Nature. 2003; 3:650-663.
5- Sociedad Argentina de Hematología. Guías de Diagnóstico y Tratamiento. Leucemias agudas. 2021.
Para mayor información o consultas:
 Sección: Biología Molecular
Sección: Biología Molecular
Lic. Analía Seravalle
Tel: 0341-486-1600. Int: 242

