La preeclampsia (PE) es una complicación grave del embarazo caracterizada por hipertensión y proteinuria después de la 20ª semana de gestación. Ocurre en el 3 al 5 % de los embarazos y produce morbimortalidad en la madre, el feto o el neonato. Las manifestaciones clínicas van desde formas ligeras hasta severas. Si la preeclampsia no se diagnostica y no se controla, puede provocar complicaciones potencialmente mortales como la eclampsia o el síndrome HELLP (del inglés, hemolysis, elevated liver enzimes, low platelets count) (1).
La PE se concibe como un trastorno que se establece en dos fases: la primera consiste en el establecimiento de una deficiente circulación placentaria durante la mitad inicial del embarazo que condiciona un estado de hipoxia placentaria, y la segunda en la aparición de una respuesta sistémica materna durante la mitad final de la gestación caracterizada por un exceso de factores antiangiogénicos.
El factor de inicio en PE sería la reducción de la perfusión útero placentaria, como resultado de la invasión anormal de las arterias espiraladas por el trofoblasto. Durante la implantación placentaria normal, los citotrofoblastos migran hacia las arterias espiraladas uterinas maternas formando senos vasculares en la interfaz fetal-materna para proporcionar nutrición al feto. En las placentas destinadas a desarrollar preeclampsia, los citotrofoblastos fallan en la invasión causando la remodelación incompleta de las arterias espiraladas. Esto conduce a vasos maternos estrechos, aumento en la resistencia vascular sistémica, presencia de reactividad vascular y modificación en la distribución del flujo sanguíneo en la pelvis, todo lo cual precede al inicio de la hipertensión.
Los efectos de esta alteración se manifiestan cuando los requerimientos nutricionales para el desarrollo fetal comienzan a superar la capacidad placentaria para suministrar la cantidad de flujo sanguíneo necesario. Se produce una situación de progresiva hipoxia placentaria en la que la placenta reacciona liberando a la circulación una serie de sustancias responsables de la disfunción endotelial sistémica materna que caracteriza a la PE.
El cuadro clínico es desencadenado por la disfunción de las células endoteliales junto a otras alteraciones vasculares como la vasoconstricción, el aumento de la permeabilidad capilar y la agregación plaquetaria. En PE, existe un desequilibrio en la producción y liberación a la circulación materna de factores reguladores de la angiogénesis desde la placenta en situación de isquemia.
Uno de los factores es la forma soluble de la tirosina quinasa 1 (sFlt-1). Esta proteína actúa como un potente factor antiangiogénico endógeno antagonista de dos factores proangiogénicos como el factor de crecimiento endotelial vascular (VEGF) y el factor de crecimiento placentario (PlGF), que se adhiere a los dominios de unión de PlGF y VEGF, variando la configuración de estas proteínas. Esta situación impide su interacción con los receptores endoteliales de superficie y por tanto induce la disfunción endotelial. (2,3)
Tamizaje en 1er trimestre.
El objetivo de este estudio es identificar a las mujeres con embarazo de riesgo de modo de prevenir la aparición de la enfermedad, y poder tratarlas en forma precoz para mejorar los resultados obstétricos y perinatales.
El enfoque tradicional para la detección de PE es identificar los factores de riesgo en base a las características maternas y el historial médico (factores maternos).
Un enfoque alternativo permite la estimación de riesgos de PE mediante un screening que combina el riesgo a priori de los factores maternos con marcadores clínicos (tensión arterial media), marcadores ecográficos (Doppler de arterias uterinas; la pulsatilidad (IP) aumentada puede detectarse desde el primer trimestre de embarazo, aunque tiene mayor sensibilidad en el segundo trimestre y es el marcador más sólido a incluir en los test) y marcadores bioquímicos (PlGF).
Según la inclusión de estos parámetros en el test de screening se obtiene una tasa de detección aproximada de un 90% de PE <32 semanas, 75% de PE <37 semanas y 43% de PE ≥37 semanas, con una TFP del 10% (4).
Cociente sFlt-1/PlGF.
El gold estándar actual para las evaluaciones diagnósticas incluye la determinación de presión arterial (PA) y proteinuria. Estos carecen de sensibilidad y especificidad para evaluar la gravedad de la enfermedad o predecir su progresión. Además, son marcadores tardíos ya que se presentan cuando la patología ya está instalada.
En mujeres con PE están alteradas las concentraciones séricas del PIGF y sFlt 1. En gestaciones normales, el factor proangiogénico PIGF aumenta durante los primeros dos trimestres para reducirse posteriormente a medida que el embarazo alcanza su término. Las concentraciones del factor antiangiogénico sFlt 1, al contrario, permanecen estables durante las fases inicial e intermedia, pero se incrementan permanentemente hasta el término de la gestación. En las mujeres que desarrollan preeclampsia, las concentraciones de sFlt 1 son más altas y las concentraciones de PlGF más bajas que en un embarazo normal.
En pacientes con factores de riesgo, signos o síntomas de preeclampsia, el cociente sFlt 1/PlGF resulta útil en la predicción a corto plazo de la enfermedad. Un cociente elevado se asocia con un mayor riesgo de preeclampsia.
Una relación sFlt-1/PlGF de 38 o menos descarta PE dentro de 1 semana con un valor predictivo negativo de 99.3% para cualquier edad gestacional; un valor de índice entre 38 – 85 predice la presencia de PE dentro de las 4 semanas con un valor predictivo positivo 36,7%. Un valor mayor a 85, presenta alto riesgo de desarrollo de PE en forma inmediata. (5)
Valores más altos de cociente se asocian con desarrollo de complicaciones severas tanto en la madre como en el feto; aumenta significativamente el riesgo de parto prematuro y está asociado con la ocurrencia de resultados adversos tanto maternos, fetales como en el RN.
La capacidad de descartar con precisión PE sobre la base del sFlt-1/PlGF mejora las decisiones clínicas con respecto a la hospitalización y la intensidad de la monitorización ambulatoria. En la práctica clínica, un valor predictivo negativo muy alto es crucial en la evaluación de una paciente con sospecha de preeclampsia, ya que no detectar la enfermedad inminente podría tener consecuencias importantes para el feto o la madre.
Prestaciones disponibles en Cibic:
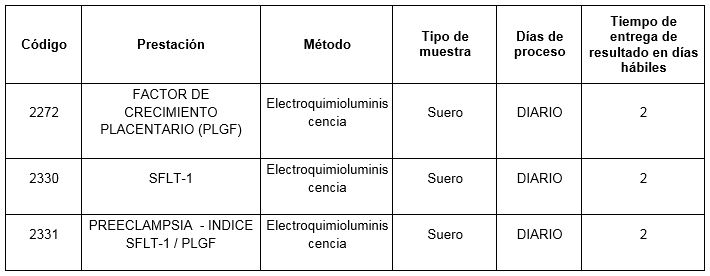
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la extranet.
Referencias
1-Uzan J, Carbonnel M, Piconne O, et al. Pre-eclampsia: pathophysiology, diagnosis, and management. Vasc Health Risk Manag 2011;7:467-47.
2-PlGF-based testing to help diagnose suspected pre-eclampsia (T suspected pre-eclampsia (Triage PlGF riage PlGF test, Elecsys immunoassa test, Elecsys immunoassay sFlt-1/PlGF y sFlt-1/PlGF r ratio, DELFIA Xpress PlGF 1-2-3 test, and ratio, DELFIA Xpress PlGF 1-2-3 test, and BRAHMS sFlt-1 .
3-Sarosh Rana, Elizabeth Lemoine, Joey Granger, S. Ananth Karumanchi. Preeclampsia. Pathophysiology, Challenges, and Perspectives. AHA journal. 2019;124:1094–1112.
4-N. O’Gorman y cols. Multicenter screening for pre-eclampsia by maternal factors and biomarkers at 11–13 weeks’ gestation: comparison with NICE guidelines and ACOG recommendations. Ultrasound Obstet Gynecol 2017; 49: 756–760.
5-Harald Zeisler y cols. Predictive Value of the sFlt-1:PlGF Ratio in Women with Suspected Preeclampsia. The New England Journal of Medicine. 2016. Vol374 n°1.
Para mayor información o consultas:
Producción Bioquímica Clínica
Bioq. Santiago Di Vita
Tel: 0341-4722424. Int: 215
Sección: Producción Bioquímica Clínica
Bioq. Ma. Florencia Mora Dengra
Tel: 0341-4722424. Int: 221

