El Virus Sincicial Respiratorio (VSR) es un virus de cadena simple de ARN, miembro de la familia Paramyxoviridae, subfamilia Pneumovirus. Desde su descubrimiento en 1956 se reconoce como una de las causas más comunes de enfermedad en la infancia.
El VSR tiene un único serotipo con dos subgrupos antigénicos, VSR-A y VSR-B que co-circulan durante el año con mayor incidencia desde el invierno a la primavera, siendo el VSR-A el más común (1). En Argentina, dentro de los agentes virales identificados en la totalidad de muestras positivas para virus respiratorios, desde enero hasta julio de 2017, el 63% correspondió a Virus Sincicial Respiratorio, con un aumento marcado y sostenido desde el mes de abril. Estos casos se concentran en CABA, Buenos Aires, Córdoba, Tucumán, Santa Fe, Salta y Chaco (2).
El VSR es la causa más frecuente de infecciones respiratorias agudas en lactantes y niños pequeños y usualmente involucra el tracto respiratorio superior causando fiebre, congestión nasal, rinorrea y tos. Sin embargo, aproximadamente el 40% de las infecciones primarias de VSR resultan en infecciones respiratorias del tracto inferior, principalmente bronquiolitis y neumonía, siendo la causa más común de las mismas en niños menores de 2 años, requiriendo de internación en algunos casos (2 y 3).
En nuestro país, luego de las afecciones perinatales y las malformaciones congénitas, las infecciones respiratorias agudas bajas constituyen la causa más frecuente de muerte en los menores de 1 año y ocupan el cuarto lugar en el grupo etario de 1 a 4 años, luego de los accidentes, y las anomalías congénitas (4).
El VSR está siendo reconocido también como una causa cada vez más importante de infecciones respiratorias en adultos. Estudios epidemiológicos sugieren que la población adulta con mayor riesgo de sufrir enfermedades más severas incluye a adultos con enfermedades cardiopulmonares de base, ancianos e inmunocomprometidos (5).
Dado que aún no se cuenta con vacunas contra el VSR, el interés en los últimos años se concentró en la profilaxis pasiva con un anticuerpo monoclonal llamado Palivizumab que demostró ser seguro y efectivo para disminuir en forma significativa la internación por infecciones respiratorias bajas por VSR (6). Las opciones de tratamiento son limitadas ya que el único antiviral con licencia es la ribavirina pero su eficacia en pacientes con factores de riesgo no está bien establecida, tiene muy poco beneficio y no se usa de rutina (7).
Se ha demostrado que en los adultos, los títulos virales son bajos en secreciones nasales y respiratorias bajas, en contraste con los niños en los que tienen altos títulos virales en secreciones nasales (8). De este modo, la detección del VSR en secreciones respiratorias por inmunofluorescencia, método con una sensibilidad del 75-95% en niños, es aún menos útil en adultos mayores.
Por su alto rendimiento, automatización aumento de sensibilidad y la disminución significativa del tiempo de obtención de resultados, la detección de ácidos nucleicos está emergiendo como el método diagnóstico de preferencia para las infecciones respiratorias (1).
La detección rápida del VSR es sumamente necesaria para definir el manejo clínico del paciente, aplicar una terapia temprana, tomar las medidas de control de la infección apropiadas para prevenir la transmisión nosocomial durante el período estacional de mayor hospitalización y hasta disminuir los costos asociados al cuidado del paciente.
A su vez, la subtipificación de VSR es importante para fines epidemiológicos, permitiendo evaluar la prevalencia y la patogenicidad de cada subgrupo de VSR, así como su sensibilidad a los tratamientos.
En Cibic hemos desarrollado un ensayo de PCR en tiempo real que permite la detección de ARN del VSR y la identificación en los dos subgrupos VSR-A y VSR-B de forma rápida, sensible y específica.
Determinaciones disponibles en Cibic:
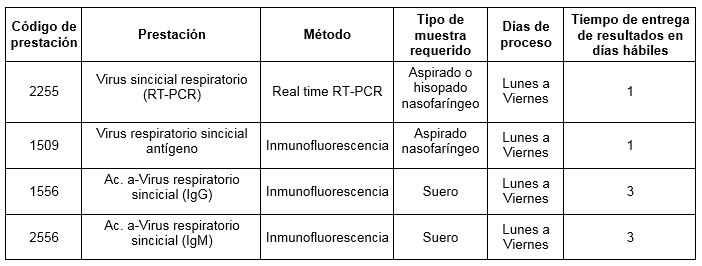
Para conocer las condiciones del paciente, de almacenamiento y de envío de las muestras y otros datos sobre las prácticas consulte al manual de prestaciones.
Referencias:
1-Somerville L. et al. (2015) Molecular diagnosis of respiratory virus. Pathology 47(3): 243–249).
2-Ministerio de Salud de la Nación, Dirección de Epidemiología-Boletín Integrado de Vigilancia N° 368 – SE 28- 2017)
3-Paes B et al. (2011) A decade of respiratory syncytial virus epidemiology and prophylaxis: Translating evidence into everyday clinical practice. Can Respir J 18: e10.
4- Ministerio de Salud de la Nación. Dirección de Estadísticas e información de Salud. http://www.deis.msal.gov.ar/wp-content/uploads/2016/12/Serie5Numero59.pdf
5- de-Paris F. et al. (2012) Optimization of one-step duplex real-time RT-PCR for detection of influenza and respiratory syncytial virus in nasopharyngeal aspirates. Journal of Virological Methods 186 189– 192.
6- Comité de Estudios Feto-Neonatales, Comité de Infectología, Comité de Neumonología (2000) Recomendaciones sobre el uso de palivizumab. Arch. Argent. Pediatr 98:348-349.
7- Ventre K et al. (2007) Ribavirin for respiratory syncytial virus infection of the lower respiratory tract in infants and young children. Cochrane Database Syst Rev. 24:CD000181.
8- Falsey A et al. (2000) Respiratory Syncytial Virus Infection in Adults Clin Microb Rev 13: 371-384
Para mayor información o consultas:
 Sección Biología Molecular
Sección Biología Molecular
Mariela Sciara, Dra. en Ciencias Biológicas.
Tel: 0341-4499444. Int: 225.
 Sección Bioquímica Clínica No Automatizada
Sección Bioquímica Clínica No Automatizada
Bioq. Franco Delleppiagge
Tel: 0341-4499444. Int: 222

