El análisis citogenético clásico o cariotipo por bandeo G desempeña un papel importante en el estudio de las anomalías cromosómicas constitucionales y adquiridas. Permite la detección de grandes alteraciones genómicas, incluidas aneuploidías, reordenamientos estructurales cromosómicos equilibrados y desequilibrados de al menos 5 – 10 Mb de tamaño, como también mosaicismos (1). Sin embargo, la necesidad de trabajar con células en división, a veces una morfología cromosómica deficiente, y la resolución, en ocasiones, relativamente baja del bandeo G son factores limitantes para un estudio completo y preciso de los cromosomas (1).
La Hibridación in situ Fluorescente o FISH, por sus siglas en ingles, ha permitido superar estas limitaciones. El FISH es una técnica que detecta secuencias de ADN en células o tejidos preservados mediante el empleo de una sonda (fragmento de ADN homólogo a la secuencia blanco) marcada con un fluorocromo, la cual va dirigida hacia un lugar específico del ADN y que emite fluorescencia que puede ser observada por medio de un microscopio de epifluorescencia. Esta se fundamenta en la capacidad que poseen los ácidos nucleicos para hibridarse entre sí, es decir, la existencia de determinada secuencia de ADN, que resulta complementaria con otra secuencia (2).
Esta técnica ha demostrado ser de gran valor para la identificación de aberraciones cromosómicas clínicamente significativas, ya que el FISH se puede realizar en metafases o células en interfase que no se dividen, y puede detectar anormalidades genómicas con una resolución de 150 a 900 kb dependiendo del tamaño de la sonda (1).
Según el diseño de la sonda de hibridación específica, el FISH puede ser: centromérico (ADN alfa satélite), locus específico, subtelomérico de brazos cortos y/o largos, de pintado cromosómico (hibrida en todo el cromosoma) (1). Existen técnicas de FISH más complejas que por combinación de sondas marcadas con diferentes fluorocromos se combinan permitiendo identificar cada cromosoma de un color distinto (Cariotipo Espectral) o bien cada banda de un solo cromosoma (Multibanding). Estas técnicas sirven para resolver anomalías complejas y/o cromosomas marcadores, no identificables por las técnicas citogenéticas convencionales (2, 3).
Su principal ventaja es que puede aplicarse sobre células en interfase y facilita su análisis sobre un mayor número de células. Además de ser una técnica más sensible y especifica. FISH es una herramienta clave para confirmar el resultado de un cariotipo previo o muchas veces definir el diagnóstico. A pesar de las numerosas ventajas, la técnica de FISH no proporciona análisis de todo el genoma y debe estar dirigido a regiones genómicas seleccionadas que se consideran de interés en un caso dado (2).
Se aplica habitualmente en la detección de pequeñas deleciones y duplicaciones que no son visibles por el análisis microscópico habitual. Síndromes como Prader-Willi / Angelman (ver figura 1), Williams, Smith-Magenis y Velocardiofacial/ DiGeorge son muy difíciles de visualizar en cromosomas metafásicos por bandeo G convencional, el FISH se ha convertido en la técnica de elección cuando se sospecha un síndrome por microdeleción/ duplicación (2). Además permite detectar anomalías numéricas (aneuploidías) y es una herramienta importante para confirmar reordenamientos cromosómicos que se sospechan después de la evaluación citogenética. La técnica de FISH permite detectar bajos niveles de mosaicismo, muy útil en casos con cariotipo normal en sangre periférica. Actualmente las técnicas de citogenética molecular como CGH array, FISH y las técnicas de cariotipo convencional (bandeo G) se usan de manera complementaria para realizar el estudio de anormalidades constitucionales en un individuo (1, 2).
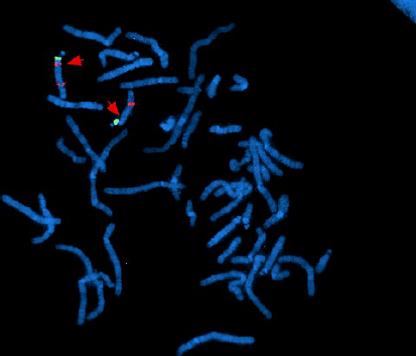
Figura 1: Deleción constitucional 15q13. Sonda SNRPN (roja)/PML (roja)/CEP 15 (verde) para Prader-Willi /Síndrome de Angelman: este paciente tiene una microdeleción en la región 15p13. El cromosoma normal (15) exhibe un señal verde (CEP 15) y una señal (PML) roja (sondas de control para verificar la región pericentromérica de 15 y la 15q distal), y una señal de SNRPN roja proximal al centrómero en el brazo largo. El cromosoma 15 con la deleción exhibe solo las señales control (PML y CEP 15), le falta la señal roja de la sonda SNRPN (flecha). Adaptado de The AGT Cytogenetics Laboratory Manual (2017). 4th Edition. Wiley-Blackwell.
Otra área de aplicación del FISH es en el diagnóstico, pronóstico y seguimiento de neoplasias hematológicas. La metodología de FISH permite la detección rápida de genes de fusión susceptibles de terapia dirigida (PML-RARA, BCR-ABL (ver figura 2)); otras anormalidades citogenéticas recurrentes de importancia diagnóstica o pronóstica que pueden estar presentes en las células quiescentes, deleciones, reordenamientos cromosómicos y anomalías en el número de copias; mosaicismo de nivel relativamente bajo para aberraciones clonales mediante la evaluación de una gran población de células interfásicas. Además puede facilitar la caracterización de reordenamientos cromosómicos complejos identificados mediante análisis cromosómico de rutina (3)
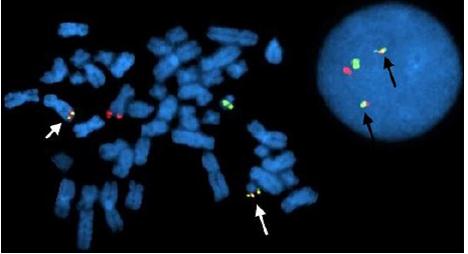
Figura 2: Sonda de fusión para FISH BCR / ABL1, t (9; 22). Célula en metafase e interfase con sonda de doble fusión que muestra una señal roja (normal 9), verde (normal 22), fusión sobre der (9) y fusión sobre der (22), ambos aparecen de color amarillo. Adaptado de The AGT Cytogenetics Laboratory Manual (2017). 4th Edition. Wiley-Blackwell.
En resumen, la técnica FISH constituye una invaluable herramienta clínica que brinda información clave en el estudio de alteración genéticas adquiridas y constitucionales. Sumado a la información aportada por las otras técnicas de citogenética molecular y al cariotipo convencional aportan datos importantes para el estudio de las enfermedades genéticas y procesos oncohematológicos.
Prestaciones disponibles en Cibic:
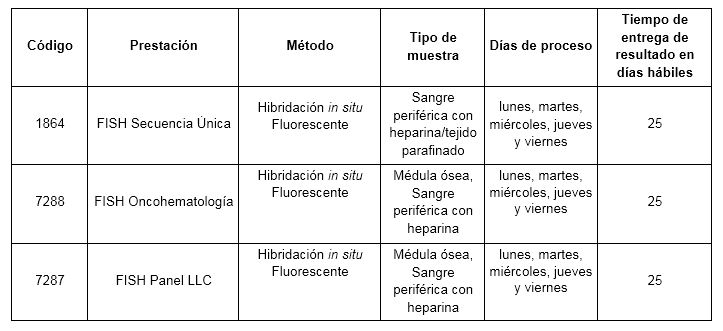
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la extranet.
Bibliografía
1. Arsham MS, Barch, MJ Lawce HJ. (2017). The AGT Cytogenetics Laboratory Manual. 4th Edition. Wiley-Blackwell.
2. Gersen SL, Keagle MB. (2013). The Principles of Clinical Cytogenetics. USA. Humana Press.
3. Zneimer, S. M. (2016). QUALITY MANAGEMENT, in Cytogenetic Laboratory Management: Chromosomal, FISH and Microarray-Based Best Practices and Procedures, John Wiley & Sons, Inc., Hoboken, NJ, USA.
Para mayor información o consultas:
Sección: Citogenética.
Dr. Carlos Zumoffen.
Tel: 0341-4499444 interno 283.
