La leptospirosis es una zoonosis de amplia distribución geográfica que aparece en forma aislada o en brotes epidémicos estacionales.
El agente etiológico es una espiroqueta del género Leptospira. El género incluye 11 especies. La única especie patógena para el ser humano es Leptospira interrogans. Poseen 1-2 flagelos, 30 a 50 espiras muy pequeñas y apretadas. Su espesor es 0,1 µm por lo que sólo son visibles con microscopio con campo oscuro. Los extremos son incurvados en forma de ganchos y es posible cultivarlos. Además, poseen antígenos superficiales que generan anticuerpos protectores que sirven también para clasificarla en serovariedades, y antígenos profundos propios de la especie. Existen más de 210 serovars (L. icterohemorragica, L. autumnalis, L. bataviae, L. canicola, L. pomona, etc.).
La leptospirosis es una zoonosis ya que afecta numerosos animales, como roedores, perros (reservorios en áreas urbanas) y animales de cría, bovinos, ovinos, porcinos, equinos, caprinos, que eliminan el microorganismo por la orina contaminando fuentes de agua donde puede vivir varias semanas.
Epidemiología:
La cantidad de casos se incrementa con el aumento de lluvias y temperatura, aunque puede ocurrir a lo largo de todo el año. Los brotes de leptospirosis suelen aparecer luego de desastres naturales tales como inundaciones y huracanes.
En nuestro país, las exposiciones que ocurren durante las inundaciones se consideran el principal factor de riesgo para la leptospirosis. Las provincias con mayor notificación pertenecen a la región centro: Entre Ríos, Santa Fe y Buenos Aires, aunque la enfermedad está distribuida en todo el país.
Es también una enfermedad profesional afectando a trabajadores de establos, mataderos, curtiembres, veterinarios, carniceros, pescadores y arroceros.
Modo de infección y manifestaciones clínicas:
Las leptospiras ingresan a través de la piel erosionada o de las mucosas orofaríngea, nasal, ocular, aunque también pueden penetrar por la piel íntegra si permanece inmersa en agua por un tiempo.
El espectro de la enfermedad es muy amplio: varía desde episodios febriles inespecíficos autolimitados hasta formas graves con insuficiencia renal o hemorragia pulmonar cuya tasa de letalidad puede alcanzar el 50%.
Entre las personas que desarrollan la enfermedad, se distinguen diferentes formas clínicas:
a) Leptospirosis anictérica (90%de los casos), que se presenta como un síndrome febril inespecífico.
b) Leptospirosis ictérica o Síndrome de Weil (5-10%), que presenta diversos grados de compromiso sistémico: insuficiencia renal, meningitis, neumonía, manifestaciones hemorrágicas.
c) Síndrome pulmonar hemorrágico grave.
Pruebas de laboratorio:
El diagnóstico de la leptospirosis se basa principalmente en la detección directa de leptospiras o de anticuerpos frente a las leptospiras en muestras del paciente.
Durante la primera fase, llamada fase febril o leptospiremia, se pueden detectar las leptospiras en la sangre, en el líquido cefalorraquídeo y en la mayoría de los tejidos del cuerpo. Como la concentración de leptospiras en este tipo de muestras puede ser baja, cuando se sospecha leptospirosis es necesario recoger varias muestras del paciente. Estas muestras pueden cultivarse en medios especiales para leptospira y después de multiplicarse se pueden llegar a ver mediante un tipo de microscopía denominada de fondo o campo oscuro. Como estas técnicas son complicadas y, en ocasiones, se necesita un tiempo largo para ver el resultado, la mayoría de los laboratorios no cultivan las leptospiras y se centran en la detección de los anticuerpos frente a leptospiras. En algunos laboratorios se utiliza también la técnica de reacción en cadena de polimerasa (PCR) para la detección de material genómico de leptospira en muestras de pacientes.
Los anticuerpos frente a las leptospiras aparecen entre 5 y 7 días después, y se pueden detectar mediante técnicas de laboratorio. La prueba de detección de anticuerpos de referencia es la aglutinación microscópica o MAT (microscopic agglutination test), que consiste en mezclar el suero del paciente con leptospiras y posteriormente examinar en el microscopio la aglutinación. Debido a que la MAT se realiza con microorganismos vivos, muy pocos laboratorios la realizan. En su lugar se utilizan primerametne técnicas de enzimoinmunoanálisis (ELISA) para la detección de anticuerpos IgM e IgG que sirven para un primer cribado (los casos positivos se deberían confirmar con la prueba MAT en un laboratorio de referencia). La presencia de estos anticuerpos sirve para el diagnóstico de la fase inmune.
A partir de la aparición de los anticuerpos, el sistema inmune lucha contra las leptospiras hasta que las bacterias dejan de detectarse en la sangre y empiezan a eliminarse por la orina. Este estadio se denomina fase de leptospiruria (es decir, leptospiras en la orina) y puede durar semanas o meses.
Prestaciones disponibles en Cibic:
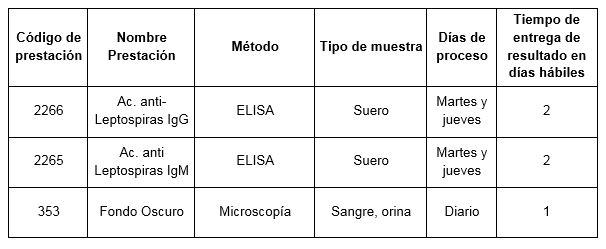
Para conocer las condiciones del paciente, de almacenamiento y envío de la muestra y otros datos sobre las prácticas consulte el manual de prestaciones y la extranet.
Bibliografía
1. Loffler SG et al. Genotypes of pathogenic Leptospira spp isolated from rodents in Argentina. Mem Inst Oswaldo Cruz 2014; 109:163-7
2. Varni V et al. Reassessment of MLST schemes for Leptospira spp. typing worldwide. Infect Genet Evol 2014; 22:216-222.
3. Notario R. Microbiología para el Médico. UNR editora. 2ª ed. Rosario 2013
4. Diagnóstico de leptospirosis: guía para el equipo de salud. Boletín del Ministerio de Salud de la Nación. 2014.
Para mayor información o consultas:
Sección: Producción Bioquímica Clínica No automatizada.
Bioq. María Florencia Mora Dengra.
Teléfono: 0341- 4499444. Interno: 220/ 222.

