El Screening o Pesquisa Neonatal consiste en realizar un análisis a todos los recién nacidos para detectar al posible portador de una enfermedad severa. Resulta de fundamental importancia en aquellas enfermedades que carecen de síntomas específicos tempranos, que producen daño severo e irreversible y que son pasibles de tratamiento.
De esta forma el objetivo del Screening Neonatal es la detección temprana del bebé afectado, para tratarlo en los primeros días de vida y evitar el daño neurológico.
La Ley Nacional Nº 26.279 establece la obligatoriedad del diagnóstico, tratamiento y seguimiento de las siguientes patologías:
• Fenilcetonuria (PKU)
• Hipotiroidismo Congénito (HC)
• Fibrosis Quística (FC)
• Hiperplasia Suprarrenal Congénita (HSC)
• Galactosemia (GAL)
• Déficit de Biotinidasa
¿Cuándo debe realizarse la toma de muestra para la pesquisa neonatal?
Se tomará la muestra mediante punción del talón a todo niño recién nacido entre las 48 horas y el 5º día de vida, por lo menos 24 horas después de que el niño haya comenzado a alimentarse.
Para la detección de Fenilcetonuria y Galactosemia, el niño debe estar recibiendo alimentación láctea (materna o artificial) durante por lo menos 24 horas al momento del examen.
Si la toma de muestra se realiza antes de lo indicado, se pueden presentar falsos positivos en las pruebas de HC e HSC y lo que es más grave aún, falsos negativos en la pesquisa de Galactosemia y PKU.
Si la recolección se realiza luego del 5° día de vida, considerar:
– La efectividad del tratamiento disminuye con el tiempo de implementación.
– La Pesquisa de FQ pierde valor diagnóstico luego de los 30 días de vida, pasado este tiempo debe realizarse el Test del Sudor.
– Se corre el riesgo de que los niños afectados por las formas severas de HSC y GAL sufran daño severo o inclusive la muerte durante las 2-3 primeras semanas de vida.
A pesar de que el screening neonatal se realiza desde hace casi 50 años y no obstante su aparente sencillez, es frecuente que los laboratorios reciban muestras en papel de filtro mal tomadas, inadecuadas para el procesamiento analítico de buena calidad. Cuando el laboratorio recibe un espécimen inadecuado, debe solicitar otro, y hay que repetir el proceso. Estas muestras de mala calidad elevan el costo del screening, causan trauma innecesario a los recién nacidos, producen ansiedad en los padres, potencialmente retrasan el diagnóstico y el inicio del tratamiento de los niños afectados y lo más grave, es que pueden contribuir a pasar por alto casos con un error innato del metabolismo.
Por lo anterior, es importante que el personal de salud involucrado con el screening neonatal conozca los fundamentos de la toma de muestra de sangre del talón de los recién nacidos.
Procedimiento para la correcta toma de muestra de sangre de talón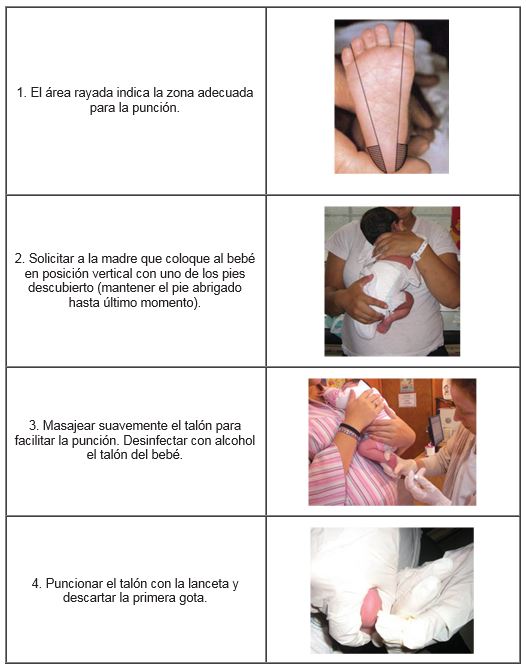
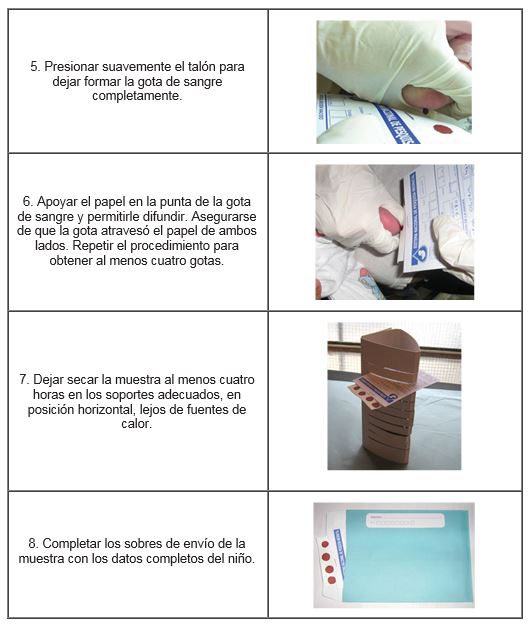
Muestra satisfactoria:
Se debe asegurar que cada círculo de la tarjeta quede completamente cubierto con una cantidad uniforme de sangre a fin de que la calidad y confianza de los ensayos no se vea comprometida por problemas en la muestra.

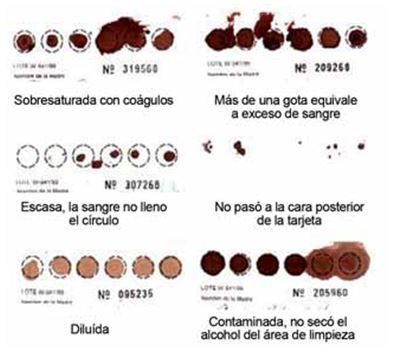
Ejemplos de muestras mal tomadas:
Las razones por la cual una muestra puede pasar a ser no válida son varias, algunas de ellas son:
• Restos de alcohol pueden diluir la muestra y afectar indirectamente los resultados.
• Apretar o exprimir la punción puede causar hemólisis y pasaje de fluido tisular a la muestra.
• Si la muestra entra en contacto con agua, fórmulas alimenticias, soluciones antisépticas, etc. debe ser descartada y repetirse.
• No guardar la tarjeta en el sobre antes de que el papel de filtro esté completamente seco.
• Un secado insuficiente o en condiciones inadecuadas afecta el resultado de la determinación.
Tarjeta de muestra
En la tarjeta de la muestra se incluyen los datos mínimos necesarios, determinados por el sistema nacional de pesquisa neonatal, para el ingreso, control y seguimiento de cada recién nacido.
Es importante que se completen en forma clara todos los campos antes de realizar la extracción.
Determinaciones disponibles en Cibic:
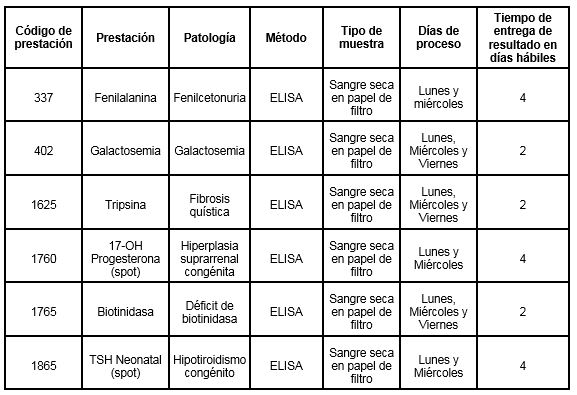
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la intranet.
Bibliografía:
1. Beutler E. Galactosemia: screening and diagnosis. Clin Biochem 1991;24:293-300.
2. Hoffman GL, Laessig RH, Jhassemer D, Makowski E. Dual-Channel Continious-Flow Systems for Determination of Phenylalanine and Galactose. Clin Chem 1984;30/2:287-90.
3. McCaman MW, Robins E. Fluorometric method for the determination of phenylalanine in serum. J Lab Clin Med 1962;59:885.
4. Yamaguchi A, Fukushi M, Mizushima Y, Shimizu Y, Takasugi N, Arashima S, et al. Microessay for Screening Newborn for Galactosemia with Use of Fluorometric Microplate Reader. Clin Chem 1989;35:9.
5. Machado C, Solís RL, Bécquer D, Cazanave J, Fernández JL. The Ultramicroanalytical System (SUMA) as a New Approach to the Newborn Screening For Hyperphenylalaninemias. En: Levy HL, Hermos RJ, Grady GF, editors. Proceedings of the Third Meeting of the International Society for Neonatal Screening; 1996, Oct 20-23. Boston, Massachusets: IKON/MAP; 1996. p.238-9.
6. Bickel HC, Bachman C, Beckers E. Neonatal mass screening for metabolic disorders. Eur J Pediatrics 1981; 137:133-9.
7. Levy HL, Simmons JR, McCready RA. Stability of Amino Acids and Galactose in the Newborn Screening Filter Paper Blood Specimen. J Pediatrics 1985;107:757-60.
8. Holton JB. A Large Scale Comparison of the Bacteriological Inhibition Assay and the Automated Fluorimetric Method for Phenylketonuria Screening. Ann Clin Biochem 1972; 9:118.
9. Fernández J.L. Pesquisa neonatal en países en vías de desarrollo. En: Cornejo V, Raimann E, Colombo M, editores. Libro de resumen IIº Congreso Latinoamericano de Errores Innatos del Metabolismo y Pesquisa Neonatal; 1999, 24-27 Octubre. Caupolicán: Servicios Gráficos; 1999. p.29.
Para mayor información o consultas:
Sección: Producción Analítica No Automatizada
Florencia Montañez
Bioq. Franco Delleppiagge
Teléfono: 0341 – 4499444. Interno: 220
