El lupus eritematoso sistémico (LES) es una enfermedad autoinmune crónica de etiología desconocida, caracterizada por diversas alteraciones inmunológicas entre las que se destacan la pérdida de autotolerancia, la activación policlonal de linfocitos B y la producción de múltiples autoanticuerpos no organoespecíficos que determinan manifestaciones clínicas diversas en prácticamente todos los órganos y sistemas. Al igual que otras enfermedades autoinmunes la etiología es multifactorial, existen: factores genéticos, factores hormonales y factores ambientales.
El LES es una enfermedad crónica multisistémica en la que cualquier órgano puede estar comprometido con variada intensidad. Afecta 10 veces más a mujeres que a hombres y es frecuente que comience con síntomas constitucionales: fiebre, fatiga, anorexia y pérdida de peso, que pueden compartirse con otras enfermedades del tejido conectivo y se deben al aumento de la producción de citocinas por el proceso inflamatorio. Son comunes en esta patología el compromiso de la piel y mucosas, presencia de artralgias o artritis y la afección renal. También se pueden encontrar poliserositis, fenómeno de Raynaud, lesiones vasculíticas, necrosis ósea aséptica, miositis de intensidad variable, manifestaciones cardiovasculares, respiratorias y neuropsiquiátricas. Algunas de estas manifestaciones pueden ser la forma de inicio o aparecer durante el curso evolutivo de la enfermedad y suelen experimentar remisiones o exacerbaciones.
En ausencia de criterios diagnósticos definidos de LES, los médicos utilizan habitualmente criterios de clasificación de LES como guía para identificar algunos de los datos clínicos más destacados cuando hacen el diagnóstico. Una de las guías más conocidas constituye la elaborada en 1982 y posteriormente revisada en 1997 por el Colegio Americano de Reumatólogos (3) la cual define 11 criterios para la clasificación de LES.
Criterios del ACR de 1982 revisados en 1997 para la clasificación de LES
1) Eritema malar
2) Eritema discoide
3) Fotosensibilidad
4) Ülceras orales o nasofaríngeas (usualmente no dolorosas)
5) Artritis no erosiva afectando a dos o más articulaciones periféricas
6) Serositis (pleuritis o pericarditis)
7) Enfermedad renal: proteinuria persistente mayor a 0,5 g/día o mayor de 3+ sino se ha cuantificado, o bien cilindros celulares (de eritrocitos, hemoglobina, granulares, tubulares o mixtos).
8 ) Enfermedad neurológica (convulsiones o psicosis)
9) Alteraciones hematológicas: anemia hemolítica con reticulocitosis ó leucopenia (<4000 mm3, en dos o más ocasiones) ó linfopenia (<1500 mm3 en dos o más ocasiones) ó trombocitopenia (<100.000 mm3).
10) Alteración inmunológicas: título anormal de anticuerpos contra DNA nativo (a-DNAn), o bien presencia de anticuerpos contra antígeno nuclear Sm (a-Sm) ó hallazgo positivo de anticuerpos antifosfolipídicos (a-cardiolipina, anticoagulante lúpico, falso positivo para test de sífilis).
11) Anticuerpos antinucleares (ANA) positivos
Para arribar al diagnóstico clínico de LES es importante que se analice la historia personal y familiar del paciente en conjunto con los hallazgos clínicos y los resultados de las pruebas de laboratorio de rutina e inmunológico.
Laboratorio de rutina:
Las pruebas en la enfermedad renal tienen un papel fundamental en la evaluación inicial del LES y en el seguimiento de recaídas y remisiones. Las anormalidades se verán reflejadas en el análisis de orina completa (sedimento patológico con cilindros) y en los analitos que evalúan función renal (uremia, creatininemia y clearance de creatinina). La proteinuria puede llegar a rangos nefróticos.
La velocidad de eritrosedimentación (VES) se encuentra aumentada por los factores plasmáticos (el aumento de anticuerpos) por lo que nos sirve como analito para definir una infección o una activación del LES.
El hemograma brinda importante información ya que la anemia que presenta esta patología es normocítica normocrómica (salvo que coexista una pérdida de hierro) pudiendo entonces presentarse como microcítica hipocrómica. La leucopenia (<4000/mm3) es acompañada en aprox. un 60% por linfopenia y se correlaciona con actividad de la enfermedad. Es infrecuente el hallazgo de leucocitosis con neutrofilia, en ese caso se debe descartar una infección intercurrente.
La trombocitopenia es una de las anormalidades más importantes en el LES debido al papel de las plaquetas en la depuración de los inmunocomplejos circulantes a través de sus receptores para Fc de IgG y complemento.
Tanto la leucopenia como la trombocitopenia pueden ser de origen autoinmune, lo que obliga a la búsqueda de anticuerpos con esa especificidad.
El análisis de los niveles del complemento (C3, C4 o CH50), los cuales tiende a disminuir cuando la enfermedad es activa, es muy útil para determinar el nivel de actividad de la enfermedad.
Laboratorio inmunológico: detección de auto-anticuerpos contra antígenos nucleares y citoplasmáticos
Los anticuerpos antinucleares (ANA) también llamados factores antinucleares (FAN) son anticuerpos, principalmente de isotipo IgG, dirigidos contra antígenos del núcleo y citoplasma de la célula eucariota. La concentración de dichos anticuerpos antinucleares está significativamente aumentada en la mayoría de los pacientes que padecen de LES así como en pacientes que padecen otras enfermedades autoinmunes.
Es posible detectar dichos auto-anticuerpos mediante la técnica de inmunofluorescencia indirecta (IFI) enfrentando al suero del paciente con células HEp-2 y analizando, en caso de reactividad, el patrón de inmunofluorescencia obtenido.
Patrones de fluorescencia de los FAN y frecuencia de presentación en LES
Los patrones de fluorescencia que dan los FAN se clasifican de acuerdo a la forma en que se distribuye la fluorescencia en el núcleo y/o en el citoplasma en: continuos (fluorescencia pareja del núcleo) y discontinuos (fluorescencia irregular, no pareja).
Los patrones continuos están relacionados con anticuerpos dirigidos a estructuras del ADN: desoxirribonucleoproteína (DNP), histonas y ADN nativo. Dichos anticuerpos dan un patrón homogéneo, aunque el a-ADNn (a-ADN nativo) también puede presentar un patrón periférico.

Los patrones discontinuos están relacionados con anticuerpos dirigidos a proteínas constitutivas de los ARNs nucleares, ARNs ribosomales y de transferencia llamadas genéricamente como Antígenos Nucleares Extraibles (ENA) presentes tanto en el núcleo como en el citoplasma. Dichos anticuerpos pueden dar patrón moteado o nucleolar.
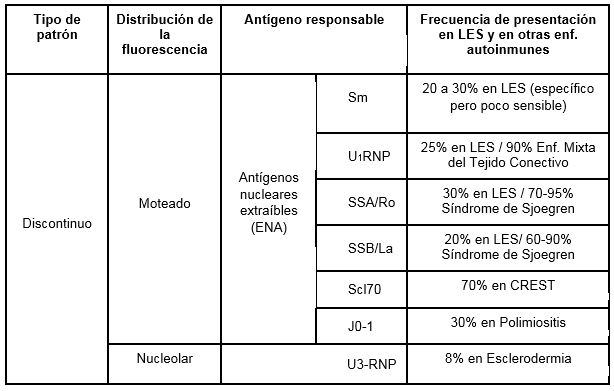
Para confirmar la especificidad del autoanticuerpo que dio un patrón de inmunofluorescencia por IFI, se deberá realizar otras prueba inmunológica de mayor especificidad como el ELISA utilizando antígenos específicos (DNAn, Sm, Ro/SSA, LA/SSB y U1 RNP).
Consideraciones importantes para interpretar los resultados de FAN
Al interpretar los resultados de FAN es importante considerar (conjuntamente con la clínica del paciente) que:
• Un test de FAN positivo por inmunofluorescencia es indicativo de LES pero no específico ya que también puede dar positivo en otras patologías autoinmunes tales como el Síndrome de Sjögren, espondilitis anquilosante, artritis reumatoidea, hepatitis autoinmune, esclerodermia, polimiositis y dermatomiositis, y también en otras condiciones no reumatoideas asociadas a daños en los tejidos tales como la enfermedad de Addison, Púrpura trombocitopénica idiopática (PTI), Enfermedad de Hashimoto, Anemia hemolítica autoinmune, diabetes mellitus tipo I, y la Enfermedad mixta de tejido conectivo.
• Pueden presentarse títulos bajos de FAN (<1/160) por IFI en un 5% de personas normales y hasta en un 30% de personas mayores de 60 años y el patrón que se presenta es usualmente moteado. También los ANA pueden detectarse en pacientes con hepatitis virales, HIV, infecciones bacterianas y en desórdenes neoplásicos como leucemias, linfomas y otros tumores. Es decir que la detección de FAN puede darse en ausencia de enfermedad reumática.
• Por otro lado, la negatividad de FAN no significa que no se esté en presencia de LES. Puede ser que la enfermedad se encuentre en remisión o que el paciente tenga una nefropatía instalada con alta proteinuria que llevó a la pérdida por orina de las inmunoglobulinas responsables del FAN positivo.
• Si el test de FAN da negativo pero la clínica igualmente sugiere fuertemente que el paciente puede padecer de LES, en tal caso, es aconsejable que se realicen pruebas adicionales utilizando antígenos específicos.
Detección de otros autoanticuerpos
También es posible que se investigue en el suero de pacientes con sospecha de LES la presencia de anticuerpos anti-fosfolipídicos tales como el anticoagulante lúpico, anticuerpos anti-cardiolipina IgG o IgM y también anticuerpos anti-beta-2-glicoproteína.
Prestaciones disponibles en Cibic:
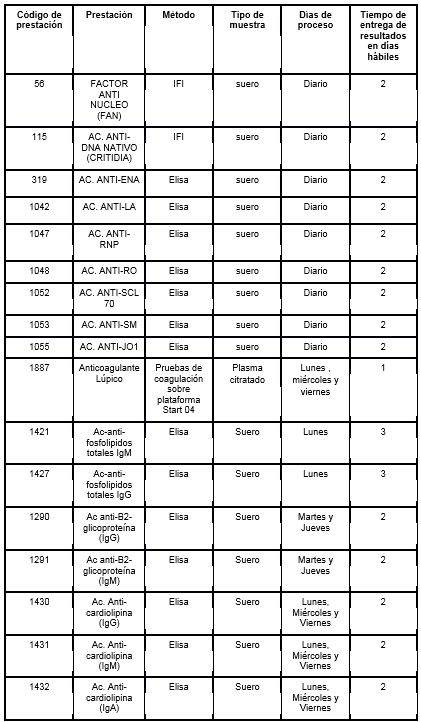
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones y a la extranet.
Bibliografía
1- Hochberg MC. Updating the American College of Rheumatology revised criteria for the classification of systemic lupus erythematosus [letter]. Arthritis Rheum 1997;40:1725. http://www.rheumatology.org/practice/clinical/classification/SLE/1997_update_of_the_1982_acr_revised_criteria_for_classification_of_sle.pdf#toolbar=1
2- Bertsias GK, Pamfil C, Fanouriakis A, Boumpas DT. Diagnostic criteria for systemic lupus erythematosus: has the time come? Nat Rev Rheumatol 2013; 9:687.
3- Petri M, Orbai AM, Alarcón GS, et al. Derivation and validation of the Systemic Lupus International Collaborating Clinics classification criteria for systemic lupus erythematosus. Arthritis Rheum 2012; 64:2677.
4- Riemakasten G and Hiepe F. Autoantibodies. In: Dubois’ Lupus Erythematosus and Related Syndromes, 8, Wallace DJ and Hahn BH. (Ed), Elsevier Saunders, Philadelphia 2013. p.282.
Para mayor información o consultas:
Sección: Producción Analítica No Automatizada
Bioq. Franco Delleppiagge
Teléfono: 0341 – 4499444. Interno: 222