La homocisteína es un aminoácido azufrado producido por la desmetilación intracelular de la metionina y exportada al plasma, por donde circula, principalmente en su forma oxidada, unida a las proteínas del plasma como la albúmina (1). También están presentes pequeñas cantidades de homocisteína reducida y el disulfuro homocisteína. La homocisteína total representa la suma de todas las formas de homocisteína encontradas en suero o plasma (libre y unida a las proteínas).
La homocisteína se metaboliza originando cisteína o metionina. Durante la transulfuración dependiente de la vitamina B6, la homocisteína se cataboliza irreversiblemente en cisteína. La mayor parte de la homocisteína se metila nuevamente formando metionina, principalmente por la enzima metionina sintetasa, que depende de la vitamina B12 y del folato. Cuando estas reacciones se alteran, la homocisteína se acumula y se excreta a la sangre (2).
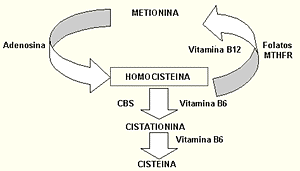
Los trastornos en el metabolismo de la homocisteína ocasionan hiperhomocisteinemia (concentraciones elevadas de homocisteína en suero o plasma) y/u homocistinuria (las concentraciones elevadas en plasma provocan que la homocisteína tenga que excretarse por la orina). La hiperhomocisteinemia está causada por deficiencias nutricionales y genéticas. La mayoría de los casos de homocisteína elevada (dos/tercios) en la población en general se debe a deficiencias de ácido fólico, vitamina B6 y vitamina B12 (3).
Se encuentran concentraciones muy elevadas de homocisteína total en individuos que padecen de homocistinuria. Se trata de un trastorno genético poco común de las enzimas relacionadas con el metabolismo de la homocisteína. Los pacientes que padecen de homocistinuria presentan retraso mental, arteriosclerosis precoz y tromboembolismo arterial y venoso (4). Existen también otras afecciones genéticas menos graves que producen concentraciones de homocisteína total moderadamente elevadas.
Se ha investigado la relación entre las concentraciones elevadas de homocisteína y los trastornos cardiovasculares, siendo la homocisteína un importante marcador para la valoración del riesgo de estas afecciones. Se ha sugerido que la homocisteína elevada es un factor de riesgo de arteriopatías coronarias, apoplejía y trombosis venosa profunda (5).
Los pacientes que padecen enfermedades renales crónicas presentan una morbimortalidad elevada debido a trastornos cardiovasculares arterioscleróticos. En la sangre de estos pacientes se observan con frecuencia concentraciones elevadas de homocisteína total. Si bien puede que estos pacientes presenten una carencia de alguna de las vitaminas relacionadas con el metabolismo de la homocisteína, las concentraciones elevadas de homocisteína total se deben principalmente a que los riñones no eliminan suficiente homocisteína de la sangre (6) (7).
Los estudios también han demostrado que la homocisteína elevada es un factor de riesgo importante en el desarrollo de diversas formas de demencia, incluyendo el Alzheimer (8). También se asocian con un riesgo elevado de padecer complicaciones en el embarazo (preeclampsia, aborto precoz recurrente, parto prematuro, bajo peso al nacer, desprendimiento de placenta o infarto). La hiperhomocisteinemia materna se asocia con defectos congénitos como anomalías del tubo neural, labio leporino y síndrome de Down (9).
A partir del Lunes 3 de noviembre la determinación de homocisteína se realizará en Cibic mediante la tecnología de inmunoanálisis quimioluminiscente (CLIA) en la nueva plataforma Architect i2000sr de Abbott (determinación cuantitativa de homocisteína total), mediante un proceso diario de dicho analito y requiriendo un menor volumen de muestra para el análisis.
Determinación disponible en Cibic:

Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte al manual de prestaciones.
Bibliografía
1. Malinow MR. Plasma homocyst(e)ine and arterial occlusive diseases: A mini-review. Clin Chem 1995;41(1):173-6.
2. Ueland PM. Homocysteine species as components of plasma redox thiol status. Clin Chem 1995;41(3):340-2.
3. Kaul S, Zaheh AA, Shah PK. Homocysteine hypothesis for atherothrombotic cardiovascular disease. JACC 2006;48(5):914-23.
4. Mudd SH, Levy HL, Skovby F: Disorders of Transsulfuration. In: Scriver CR, Beaudet AL, Sly WS, et al., editors. The Metabolic and Molecular Bases of Inherited Disease. New York: McGraw-Hill, 1995:1279-1327.
5. Lee KWJ, Hill JS, Walley KR, et al. Relative value of multiple plasma biomarkers as risk factors for coronary artery disease and death in an angiography cohort. CMAJ 2006; 174(4):461-6.
6. Guttormsen AB, Svarstad E, Ueland PM, et al. Elimination of homocysteine from plsma in subjects with endstage renal failure. Irish J Med Sci 1995; 164 (Suppl. 15):8-9.
7. Bostom AG, Lathrop L. Hyperhomocysteinemia in end-stage renal disease: Prevalence, etiology, and potential relationship to arteriosclerotic outcomes. Kidney Int 1997;52: 10-20.
8. Seshardi S, Beiser A, Selhub J, et al. Plasma homocysteine as a risk factor for dementia and Alzheimer´s disease. N Engl J Med 2002; 346(7):476-83.
9. Refsum H, Smith AD, Ueland PM, et al. Facts and recommendations about total homocysteine determinations: and expert opinion. Clin Chem 2004; 50(1):3-32.
Para mayor información o consultas:
Sección: Producción Analítica no automatizada
Bioq. Franco Delleppiagge
Tel: 0341-44994444 Interno: 220
