La prevalencia de Hepatitis C es del 3%. El 80% de los infectados progresan a infección crónica con riesgo de cirrosis y carcinoma hepatocelular. El tratamiento estándar es la administración de Interferón alfa unido a Polietilenglicol y Ribavirina (PEG IFN-Rib) durante 24 semanas para genotipos 2 o 3, y 48 semanas para genotipo 1. Este tratamiento está limitado por la falta de eficacia en muchos de los pacientes, su alto costo y numerosos efectos adversos que muchas veces requiere reducción de la dosis e incluso la suspensión prematura del tratamiento (1, 2).
La evaluación de los factores predictivos de respuesta al tratamiento es muy importante ya que permite identificar tanto a los pacientes que se beneficiarán con el tratamiento como así también evitar los efectos adversos y los costos asociados al mismo. La gran variabilidad en el transcurso de la infección por VHC y la respuesta al tratamiento se atribuye a factores virales y del hospedador.
Dentro de los factores virales, el genotipo se utiliza para predecir la respuesta al tratamiento; el 80% de los pacientes con genotipo 2 o 3 desarrollan una respuesta virológica sostenida (RVS) tras 24 semanas de tratamiento mientras que sólo el 50% de los infectados con genotipo 1 o 4 logran la RVS (3).
El advenimiento de nuevas tecnologías de secuenciación masiva, los estudios de asociación a gran escala y de asociación de genoma completo (GWAS, del inglés genome-wide association studies) han permitido, en los últimos años, avanzar en la identificación de factores genéticos del hospedador asociados con respuesta al tratamiento con Interferón alfa unido a Polietilenglicol y Ribavirina (PEG IFN-Rib) en pacientes crónicamente infectados con el virus de la Hepatitis C (VHC). Recientemente, estudios de asociación genómica han identificado los polimorfismos rs12979860 T>C y rs8099917 T>G, en el locus IL28B, asociados con la depuración espontánea y la respuesta al tratamiento del VHC con PEG IFN-Rib. El genotipo favorable CC del polimorfismo rs12979860 y el genotipo favorable TT del polimorfismo rs8099917 están asociados con 2 a 3 veces mayor tasa de RVS (TT: 33% y CT: 42% vs CC: 82% para el rs12979860, y GG: 12% y TG: 26% vs TT: 62%) (4, 5, 6, 7).
A partir de la identificación de los polimorfismos de IL28B como el factor con mayor valor predictivo de respuesta al tratamiento en pacientes infectados con genotipo 1, las principales guías de recomendaciones han incluido este test dentro del panel de determinaciones pre-tratamiento para VHC. No se ha observado el mismo efecto en los pacientes con genotipos 2 o 3. La principal utilidad de la genotipificación de los polimorfismos es la identificación, mediante el genotipo favorable (rs12979860 CC y rs8099917 TT), de pacientes infectados con VHC genotipo 1 con mayores probabilidades de lograr el éxito terapéutico. Por otro lado la ausencia de los genotipos favorables indicaría la puesta en espera del paciente a la llegada de nuevas drogas, aún más efectivas (8, 9, 10).
Muy recientemente fueron aprobados los dos primeros antivirales de acción directa, los inhibidores de la serin proteasa NS3/4A de primera generación (IP), Telaprevir (TPV) y Boceprevir (BOC), para el tratamiento de la hepatitis crónica por VHC genotipo 1. En los ensayos clínicos de fase III, la triple terapia con TPV o BOC aumentó la tasa de RVS a aproximadamente un 70% en pacientes naïve de tratamiento y permitió acortar los tiempos de tratamiento. La evidencia hasta el momento indica que el genotipo IL28B sigue siendo relevante para los resultados del tratamiento con la triple terapia para pacientes sin tratamiento previo, pero la fuerza de la asociación está atenuada. Hasta el momento la información disponible no es suficiente para determinar si la genotipificación de IL28B puede ser utilizada para recomendar la elección de un tratamiento con PEG-IFNa-Rib en lugar de un régimen basado en IP ante la presencia de un genotipo favorable (asociado con otros predictores de buena respuesta, como baja CV basal y ausencia de cirrosis) y la decisión sobre la duración del tratamiento (10).
La identificación de los polimorfismos de IL28B permite evaluar de manera individualizada a cada paciente (medicina personalizada), predecir el éxito del tratamiento y de esta manera mejorar su calidad de vida. El uso de los polimorfismos en pacientes que serán tratados con IP es aún motivo de investigación.
Determinaciones disponibles en Cibic:
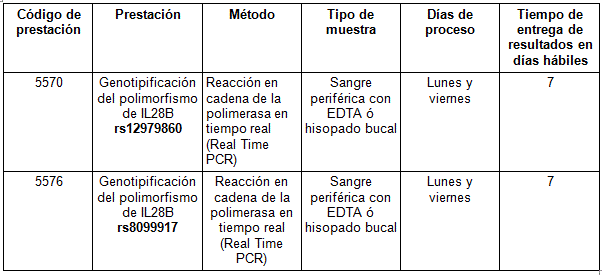
Para conocer las condiciones del paciente, de almacenamiento y de envío de la muestra y otros datos sobre las prácticas consulte a la extranet o al manual de prestaciones.
Referencias
1. Asselah, T., Rubbia-Brandt, L., Marcellin, P. & Negro, F. (2006) Steatosis in chronic hepatitis C: why does it really matter? Gut, 55, 123-130.
2. Fried, M. W., Shiffman, M. L., Reddy, K. R., Smith, C., Marinos, G., Goncales, F. L., Jr., et al. (2002) Peginterferon alfa-2a plus ribavirin for chronic hepatitis C virus infection. N Engl J Med, 347, 975-982.
3. Pawlotsky, J. M. (2003) Mechanisms of antiviral treatment efficacy and failure in chronic hepatitis C. Antiviral Res, 59, 1-11.
4. Ge, D., Fellay, J., Thompson, A. J., Simon, J. S., Shianna, K. V., Urban, T. J., et al. (2009) Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance. Nature, 461, 399-401.
5. Rauch, A., Kutalik, Z., Descombes, P., Cai, T., Di Iulio, J., Mueller, T., et al. (2010) Genetic variation in IL28B is associated with chronic hepatitis C and treatment failure: a genome-wide association study. Gastroenterology, 138, 1338-1345, 1345 e1331-1337.
6. Tanaka, Y., Nishida, N., Sugiyama, M., Kurosaki, M., Matsuura, K., Sakamoto, N., et al. (2009) Genome-wide association of IL28B with response to pegylated interferon-alpha and ribavirin therapy for chronic hepatitis C. Nat Genet, 41, 1105-1109.
7. Suppiah, V., Moldovan, M., Ahlenstiel, G., Berg, T., Weltman, M., Abate, M. L., et al. (2009) IL28B is associated with response to chronic hepatitis C interferon-alpha and ribavirin therapy. Nat Genet, 41, 1100-1104.
8. Ghany, M. G., Nelson, D. R., Strader, D. B., Thomas, D. L., Seeff, L. B. & American Association for Study of Liver, D. (2011) An update on treatment of genotype 1 chronic hepatitis C virus infection: 2011 practice guideline by the American Association for the Study of Liver Diseases. Hepatology, 54, 1433-1444.
9. Calvaruso, V. y Craxí, A. (2011) European Association of the Study of the Liver hepatitis C virus clinical practice guidelines. Liver International, 32 (1), 2-8.
10. Silva, M. O., Treitel, M., Graham, D. J., Curry, S., Frontera, M. J., McMonagle, P., et al. (2013) Antiviral Activity of Boceprevir Monotherapy in Treatment-Naïve Subjects With Chronic Hepatitis C Genotype 2/3. J Hepatol.
11. Mangia, A., Thompson, A. J., Santoro, R., Piazzolla, V., Tillmann, H. L., Patel, K., et al. (2010) An IL28B polymorphism determines treatment response of hepatitis C virus genotype 2 or 3 patients who do not achieve a rapid virologic response. Gastroenterology, 139, 821-827, 827 e821.
Para mayor información o consultas:
Sección: Biología Molecular
Lic. Analía Seravalle Tel: 0341 4499444 Int: 242
Lic. Javier Alejandro Sfalcin Tel: 0341 4499444 Int: 243
