El cáncer cérvico uterino (CCU) es la segunda causa de muerte por cáncer en mujeres, entre los 35 y 64 años, a nivel mundial. En la Argentina se diagnostican alrededor de 4.000 casos nuevos por año y mueren 2.000 mujeres por esta enfermedad (1, 2).
Se ha demostrado que la infección por el Virus del Papiloma Humano (HPV) es el factor principal para el desarrollo de neoplasia intraepitelial cervical (CIN / SIL) en mujeres, la cual es considerada una lesión precursora de cáncer cervical (3), existiendo una asociación de más del 99% entre el HPV y el cáncer de cuello de útero. La persistencia de la infección es un requisito para la progresión de CIN / SIL a cáncer. El cáncer cervical es altamente capaz de ser prevenido si se detecta en su estadio precanceroso y se procede a su tratamiento. De allí la importancia de las pruebas diagnósticas empleadas en el screening (4).
Históricamente, el tamizaje de la displasia celular a nivel del cuello uterino se realizó a través de la citología de material de cuello de útero mediante la Prueba de Papanicolaou (PAP). Aunque la citología cervical ha contribuido enormemente a la reducción de la mortalidad por cáncer cervical, su sensibilidad para detectar lesiones precursoras de cáncer es de aproximadamente del 50%, por lo que se requiere de repeticiones frecuentes para lograr una sensibilidad adecuada (1, 2). Se observó que hasta un tercio de los cáncer cervicales se producen en mujeres con 1 o más PAP negativo durante los tres años anteriores al diagnóstico (5, 6).
Debido a que la persistencia de la infección por HPV es esencial para la progresión a CIN / SIL de alto grado y a cáncer cervical, se ha sugerido la utilización de métodos de identificación de ADN de HPV para el screening inicial en reemplazo de los programas tradicionales basados únicamente en la citología (7). Los test de ADN de HPV, han demostrado mayor sensibilidad para la detección de lesiones precancerosas y cáncer cervical que la citología, permitiendo el tratamiento antes de llegar a un cáncer invasor (8).
Actualmente se han caracterizado más de 120 tipos de HPV, de los cuales 14 de ellos se consideran de alto riesgo para el desarrollo de cáncer cervical y sus lesiones precursoras (tipos 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66 y 68). Mundialmente, el 1º y 2º lugar en los genotipos más frecuentes en cáncer lo ocupan los HPV 16 y 18, respectivamente, alcanzando juntos alrededor del 70% de la etiología de las neoplasias. En América Latina y el Caribe se confirmó este hallazgo, seguidos por los tipos 31, 45, 33, 52, 58 y 35, que sumados a los HPV 16 y 18 son responsables del 86,5% de los CCU de la región (9).
La tipificación de los genotipos 16 y 18 permite identificar a las mujeres que presentan alto riesgo de CIN 3 / HSIL o neoplasia cervical invasora y proveer una estratificación del riesgo de utilidad clínica en enfermedad cervical. Las mujeres con infección por HPV 16 o 18 deben ser evaluadas a intervalos más cortos, aun en presencia de exámenes citológicos normales. En algunos casos, estas infecciones por HPV de alto riesgo oncogénico son transitorias y remiten solas, sin producir ninguna lesión epitelial (10).
Desde sus inicios, nuestro laboratorio contó con un departamento de Biología Molecular que a fines de los años 90 realizó los primeros trabajos aplicados a la detección molecular de HPV y subtipos oncogénicos. En este año 2013, CIBIC incorporó la plataforma Cobas 4800, la cual realiza la amplificación de ADN de la región L1 del HPV por medio de una PCR en Tiempo Real e hibridización de ácidos nucleicos para la detección de 14 tipos de HPV de alto riesgo en un único análisis.
Esta prueba permite identificar específicamente los tipos HPV 16 y HPV 18, además de detectar el resto de los tipos virales de alto riesgo (31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68) en un pool. Además, cuenta paralelamente con la amplificación como control interno de betaglobina para evaluar y asegurar la calidad de la muestra, identificando especímenes que contengan factores que inhiben el proceso de amplificación. Cobas 4800 es un método completamente automatizado lo que permite disminuir el riesgo de error en el proceso.
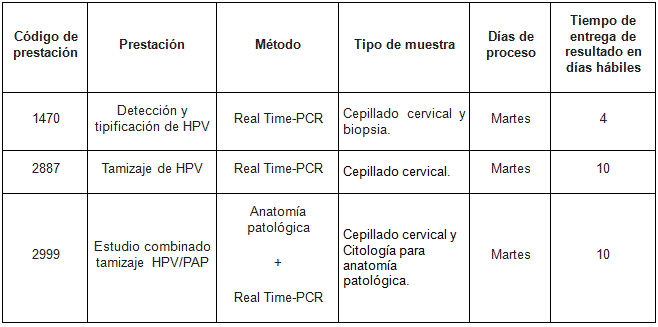
Determinaciones disponibles en Cibic:
Bibliografía
1- International Agency Cancer for Research in Cancer. Incidence and Mortality Worldwide in 2008 Globocan.
2- Schiffman, M., et al (2007). Human papillomavirus and cervical cancer. Lancet 370 (9590):890-907.
3- Bosch, F. X. et al. (2002). The causal relation between human papillomavirus and cervical cancer. J Clin Pathol 55(4): 244–265.
4- Brink A, et al. (2006) Best Practice & Research Clinical Obstetrics & Gynecology 20 (2):253-66.
5- Sun. H. Y. et al. (2000) Papanicolaou smear history and diagnosis of invasive cervical carcinoma among members of a large prepaid plan. Cancer 88:2283-9
6- Stuart, G. C. et. al. (1997). Review of the screening history of Alberta woman with invasive cervical cancer. CMAJ 157:513-9.
7- Schiffman, M., Wentzensen, N. (2010). From Human papilloma to cervical cancer. Obstet. Gynecol. 116(1):177-85.
8- Ronco et. al. (2010) Efficacy of human papillomavirus testing for the detection of invasive cervical cancers and cervical intraepithelial neoplasia: a randomised controlled trial. Lancet Oncology 11(3): 249-57.
9- Ciapponi A, et al. (2008). Prevalencia tipo-específica de virus papiloma humano en América Latina y El Caribe: una visión sistemática de estudios epidemiológicos. Congreso Argentino de Virologia, Bs As. Revista de la Asociación Argentina de Microbiologia, pag. 114.
10- POBASCAM (2004) A population-based randomized controlled trial for implementation of high-risk HPV testing in cervical screening: design, methods and baseline data of 44,102 women. Int. J. Cancer 20;110(1):94-101.
Para mayor información o consultas:
Sección: Biología Molecular
Dra. Mariana Useglio. Tel. 4499444 Interno: 241
Lic. Ezequiel Zubillaga. Tel. 4499444 Interno: 240
Dr. Marcelo Fay. Tel. 4499444 Interno: 124
